AACE là viết tắt của American Association of Clinical Endocrinology tức Hiệp hội Nội tiết Lâm sàng Hoa Kỳ. Đây là tổ chức chuyên môn lớn quy tụ các Bác sĩ Nội tiết, Chuyên gia Chuyển hóa và các nhà khoa học nhằm xây dựng hướng dẫn lâm sàng, cập nhật bằng chứng và nâng cao chất lượng chăm sóc cho người bệnh mắc các rối loạn nội tiết, bao gồm béo phì, đái tháo đường, rối loạn tuyến giáp và các bệnh lý chuyển hóa khác.
Tuyên bố đồng thuận của AACE năm 2025 cung cấp hướng dẫn trực quan dựa trên bằng chứng thông qua các lưu đồ chẩn đoán và điều trị, cùng phần tóm tắt bằng chứng nhằm hỗ trợ nhân viên y tế và người trưởng thành mắc béo phì hoặc bệnh mạn tính do mô mỡ đưa ra quyết định chung giúp nâng cao chất lượng chăm sóc và đạt được mục tiêu sức khỏe.
Lịch sử hình thành và sự phát triển của hướng dẫn AACE về quản lý béo phì
Tuyên bố đồng thuận đầu tiên của AACE về điều trị béo phì được công bố năm 1997. Các tuyên bố tiếp theo lần lượt xuất hiện vào năm 1998, 2012 và năm 2014 khi béo phì lần đầu được định nghĩa là một bệnh mạn tính.
Đến năm 2016, AACE phát hành bộ hướng dẫn và phác đồ chăm sóc toàn diện cho người sống chung với béo phì dựa trên mô hình quản lý bệnh mạn tính và khung chẩn đoán phù hợp với sinh lý bệnh của béo phì. Đây cũng là hướng dẫn đầu tiên dựa trên bằng chứng nhấn mạnh quan điểm điều trị tập trung vào biến chứng thay vì chỉ dựa vào BMI.
Hướng dẫn năm 2016 đưa ra khuyến nghị rằng, chế độ điều trị cần được điều chỉnh theo mức độ nặng nhẹ của biến chứng do mỡ thừa gây ra, không phụ thuộc BMI. BMI không thể hiện được ảnh hưởng của mỡ thừa lên sức khỏe. Hướng dẫn năm 2016 cũng bổ sung hệ thống phân tầng dựa trên nguy cơ, sự hiện diện và mức độ nặng của biến chứng như một phần của chẩn đoán. Đánh giá nhân trắc và đánh giá lâm sàng giúp phân loại chính xác mức độ bệnh từ đó định hướng mục tiêu điều trị và mức độ can thiệp phù hợp.
Năm 2017, AACE chính thức đề xuất thuật ngữ chẩn đoán bệnh mạn tính do mô mỡ, viết tắt là ABCD (adiposity based chronic disease) nhằm thể hiện rõ béo phì là bệnh mạn tính liên quan đến sự rối loạn điều hòa năng lượng và bất thường về khối lượng, phân bố cũng như chức năng mô mỡ. Hiệp hội nghiên cứu béo phì châu Âu cũng ủng hộ thuật ngữ này vào năm 2019 khi đề xuất mở rộng tiêu chuẩn chẩn đoán.
ABCD nhấn mạnh 2 yếu tố quan trọng. Một là điều gì đang được điều trị, cụ thể là sự rối loạn điều hòa năng lượng do yếu tố thần kinh nội tiết dẫn đến tích tụ mỡ bất thường. Hai là lý do phải điều trị vì đây là bệnh mạn tính có nhiều biến chứng ảnh hưởng chất lượng sống và làm tăng nguy cơ bệnh tật cũng như tử vong. Vì vậy, chẩn đoán ABCD vượt xa khái niệm béo phì chỉ dựa vào BMI.
Ủy ban Lancet về béo phì gần đây cũng phân loại “béo phì tiền lâm sàng” khi có thừa mỡ nhưng chưa xuất hiện biến chứng và “béo phì lâm sàng” khi đã xuất hiện thay đổi về cấu trúc hay chức năng cơ quan gây triệu chứng. Trong khi đó, bệnh liên quan béo phì là các bệnh thường gặp hơn ở người thừa mỡ, chia sẻ chung cơ chế sinh lý bệnh nhưng cần thêm yếu tố khác ngoài mỡ thừa mới biểu hiện.
AACE xem ABCD là thuật ngữ bao quát toàn bộ bệnh học từ giai đoạn nguy cơ, tiền lâm sàng, lâm sàng cho đến các biến chứng liên quan béo phì (obesity related complications and diseases – ORCD). Đây là cơ sở để áp dụng các biện pháp điều trị dựa trên bằng chứng xuyên suốt mọi giai đoạn từ dự phòng đến điều trị biến chứng nặng.
Béo phì là bệnh mạn tính do rối loạn chuyển hóa mang tính không đồng nhất. Đặc điểm chung là có sự tích tụ mỡ quá mức hoặc phân bố mỡ bất thường, gây nguy cơ ảnh hưởng sức khỏe. Cơ chế điều hòa năng lượng của cơ thể liên quan đến hàng loạt yếu tố thần kinh nội tiết. Béo phì hình thành do tác động qua lại giữa di truyền và môi trường, dẫn đến rối loạn cảm nhận no, thay đổi điều hòa ăn uống và tăng tích tụ mỡ.
Các quan sát lâm sàng cho thấy, cơ thể có xu hướng giữ ổn định lượng mỡ như một cơ chế sinh học. Vì vậy, sau khi giảm cân bằng thay đổi hành vi, tăng cân trở lại thường xảy ra do cơ thể kích hoạt các phản ứng chống đói và thúc đẩy dự trữ mỡ. Ngoại trừ orlistat và một số hydrogel cellulose, phần lớn thuốc điều trị béo phì hiện nay đều tác động lên các cơ chế trung ương để điều chỉnh sự tích tụ mỡ và giảm nguy cơ tăng cân trở lại sau giảm cân.

Nhu cầu cập nhật hướng dẫn 2025
Sự xuất hiện của các thuốc thế hệ mới với khả năng cải thiện sức khỏe chuyển hóa vượt trội thúc đẩy AACE cập nhật phác đồ 2025 dựa trên phác đồ năm 2016. Bản cập nhật này cũng mở rộng mô hình phân tầng của Ủy ban Lancet, phù hợp với tuyên bố đồng thuận quốc tế về giảm kỳ thị béo phì và khung chẩn đoán mới của châu Âu.
Lần đầu tiên phác đồ đưa ra hệ thống phân cấp thuốc ưu tiên cho từng biến chứng cụ thể dựa trên bằng chứng lâm sàng. Mục tiêu của tài liệu vẫn nhất quán với hướng dẫn năm 2023 về đái tháo đường típ 2 và hướng dẫn năm 2023 về kỳ thị béo phì khi nhấn mạnh điều trị cá thể hóa và chăm sóc toàn diện thay vì chỉ tập trung giảm cân.

* Voucher chỉ áp dụng cho khách hàng thăm khám lần đầu tiên tại Phòng khám MedFit
Lưu đồ chẩn đoán và các nguyên tắc trọng tâm
Lưu đồ đầu tiên gồm 9 nguyên tắc cốt lõi dành cho người trưởng thành mắc ABCD. Đây được xem là tiêu chuẩn của chăm sóc tối ưu. Nếu thiếu một trong các nguyên tắc này, kế hoạch điều trị được xem là chưa đầy đủ.

Các nguyên tắc này định hướng mô hình chăm sóc gồm đánh giá chẩn đoán toàn diện, xây dựng kế hoạch điều trị cá nhân hóa, đặt mục tiêu sức khỏe phù hợp và điều chỉnh điều trị dựa trên đáp ứng. Mọi hoạt động đều cần được thực hiện với sự thấu hiểu, tôn trọng văn hóa và xem xét các yếu tố xã hội ảnh hưởng sức khỏe.
Các lưu đồ tiếp theo mô tả mô hình điều trị tập trung biến chứng gồm quy trình sàng lọc và chẩn đoán, tiêu chuẩn đánh giá nhân trắc, phân tầng mức độ lâm sàng dựa trên biến chứng và cách dùng phân tầng này để thiết kế kế hoạch điều trị toàn diện. Điều trị phải được điều chỉnh dựa trên đáp ứng lâm sàng và chiến lược duy trì sức khỏe lâu dài.
Chẩn đoán ABCD
Chẩn đoán ABCD bao gồm 2 phần. Một là phần nhân trắc học để đánh giá mức độ tích tụ mỡ. Hai là phần lâm sàng để xác định mức độ bệnh và ảnh hưởng của mỡ thừa lên sức khỏe và chất lượng sống. Hai phần này là nền tảng để xây dựng kế hoạch điều trị cá thể hóa và chọn mức độ can thiệp phù hợp.
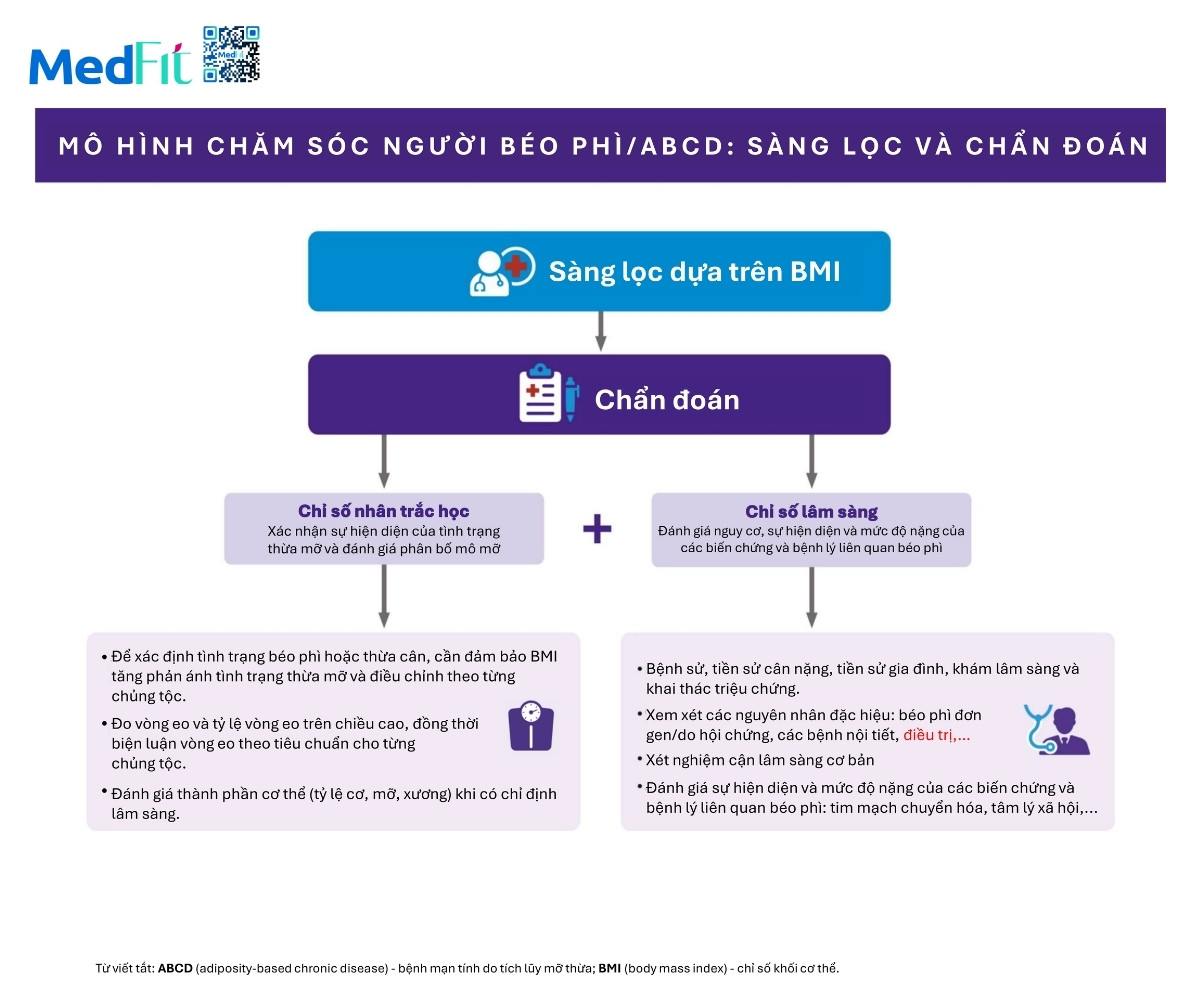
Thành phần nhân trắc
BMI phù hợp để sàng lọc ban đầu, tuy vậy tình trạng thừa mỡ cần được xác nhận bằng quan sát và thăm khám. Đánh giá khối lượng và phân bố mỡ bằng BMI và tỉ lệ vòng eo chia cho chiều cao. Việc đo tỉ lệ này cần lấy số đo vòng eo và giá trị BMI cùng vòng eo cần được diễn giải dựa trên tuổi giới tính và sắc tộc.
Những phương pháp bổ sung như hấp thụ tia X năng lượng kép gọi là DXA hoặc đo thể tích bằng trở kháng được sử dụng trong trường hợp số liệu nhân trắc hoặc kết quả thăm khám không đồng nhất hoặc không phản ánh những gì đang được ghi nhận về mặt lâm sàng. BMI cần được diễn giải trong bối cảnh lâm sàng với sự xem xét về khối cơ, phù nề, khối mô mềm và mọi yếu tố có thể làm thay đổi cân nặng ngoài phần mỡ. Cần chú ý đặc biệt đến tình trạng giảm cơ và giảm cơ kèm béo phì ở những người có nguy cơ.
Thành phần lâm sàng
Phân giai đoạn mức độ nặng của bệnh mạn tính do mô mỡ (viết tắt là ABCD) dựa trên nguy cơ sự hiện diện và mức độ nghiêm trọng của những biến chứng liên quan béo phì (viết tắt là ORCD).
Việc phân giai đoạn đòi hỏi khai thác đầy đủ về cân nặng và bệnh sử những hệ cơ quan sinh hóa chủ chốt, khi cần thì thực hiện hình ảnh học hoặc xét nghiệm chẩn đoán khác. Đánh giá lâm sàng cần sàng lọc những nguyên nhân đơn gen hoặc hội chứng các thuốc gây tăng cân, rối loạn nội tiết tố, yếu tố tâm lý xã hội và các yếu tố góp phần khác.

Sàng lọc và đánh giá
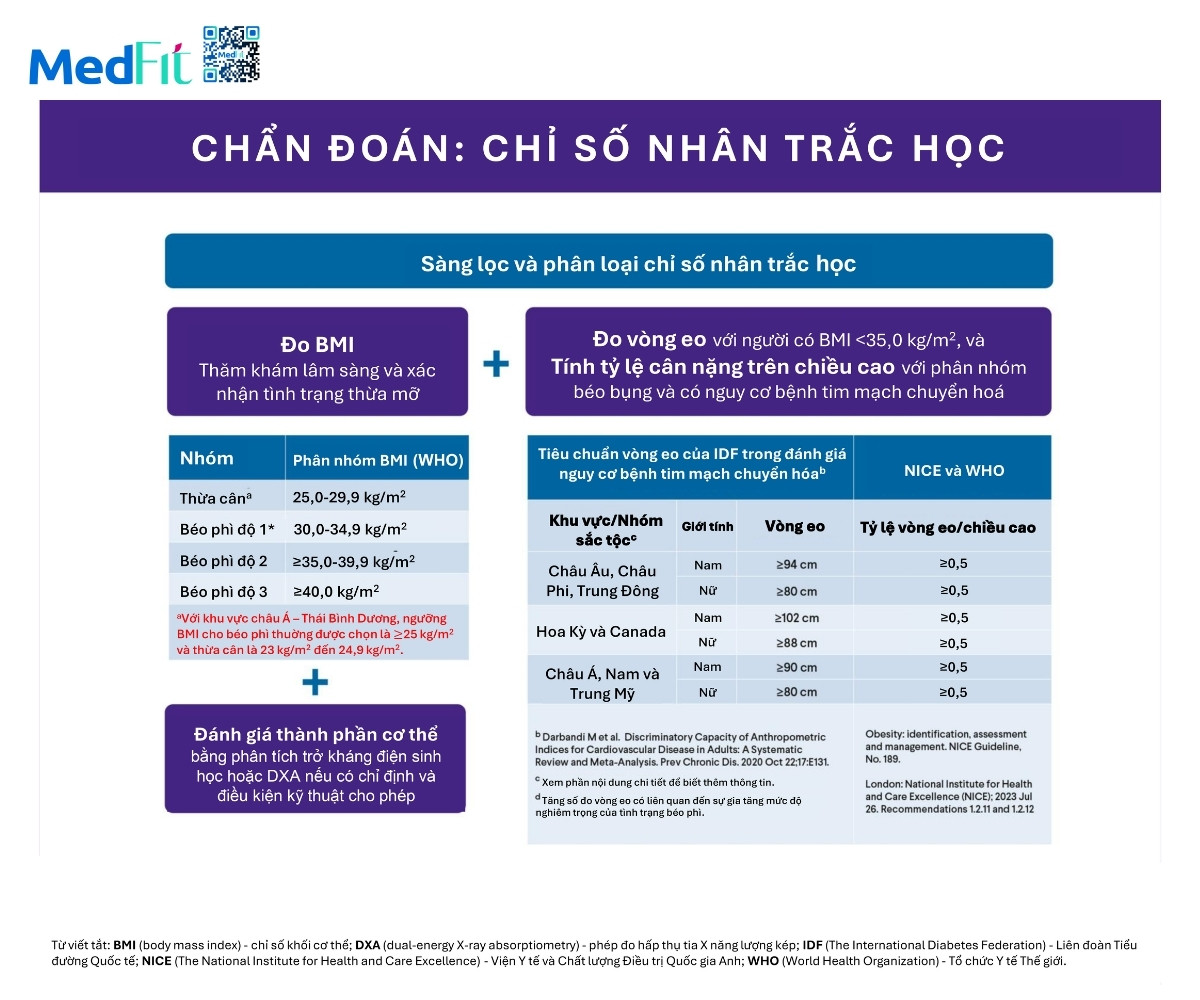
Như mô tả trong mô hình chăm sóc ở lưu đồ 2, phần nhân trắc của chẩn đoán bắt đầu bằng sàng lọc sử dụng BMI được trình bày trong lưu đồ 3. Thăm khám trực tiếp vẫn cần thiết để xác nhận sự hiện diện của thừa mỡ. Vì BMI không phản ánh phân bố mỡ nên vòng eo và tỉ lệ vòng eo chia cho chiều cao được sử dụng để đánh giá mức độ tích mỡ trung tâm, một yếu tố phản ánh sức khỏe tim mạch chuyển hóa.
Đánh giá khối lượng và phân bố mô mỡ cùng thành phần cơ thể có thể cần thêm những phương pháp ngoài thăm khám. Thành phần cơ thể có thể được đánh giá bằng DXA, trở kháng điện sinh học, chụp ảnh ba chiều hoặc cộng hưởng từ MRI nhằm tinh chỉnh độ chính xác khi cần. DXA hoặc MRI có thể sử dụng để đánh giá khối nạc hoặc thể tích cơ và mật độ khoáng xương ở những người có nguy cơ hoặc có biểu hiện liên quan đến giảm cơ hoặc giảm xương.
BMI
Sau khi xác nhận có thừa mỡ bằng thăm khám, sử dụng BMI để phân loại mức độ gồm thừa cân với BMI từ 25,0-29,9kg/m2, béo phì độ 1 với BMI từ 30,0-34,9kg/m2, béo phì độ 2 với BMI từ 35,0-39,9kg/m2 và béo phì độ 3 với BMI ≥ 40,0kg/m2. Những ngưỡng này được Tổ chức Y tế Thế giới khuyến nghị và áp dụng ở Bắc Mỹ, Nam Mỹ, châu Âu, châu Phi, hạ Sahara, Trung Đông và Úc.
Tại khu vực châu Á Thái Bình Dương, có những ngưỡng thấp hơn vì nguy cơ sức khỏe xuất hiện ở mức BMI thấp hơn. Ví dụ, Ấn Độ, Hàn Quốc và Nhật Bản sử dụng ngưỡng từ 23,0kg/m2 đến 24,9kg/m2 cho thừa cân và từ 25,0kg/m2 trở lên cho béo phì.
Tại Trung Quốc, béo phì được xác định khi BMI ≥ 28,0kg/m2 trở lên, còn thừa cân từ 24,0kg/m2 đến 27,9kg/m2. Một số nghiên cứu khác cho thấy, các ngưỡng này có thể cần điều chỉnh cho người gốc Á sống ở phương Tây. Ở người Nam Mỹ và Trung Mỹ lớn tuổi béo phì được đề xuất với ngưỡng 27,2kg/m2.
Việc diễn giải BMI cần xác nhận rằng chỉ số cao phản ánh thừa mỡ sau khi xem xét tuổi, giới tính, khối cơ, tình trạng dịch và sự hiện diện của giảm cơ hoặc giảm cơ kèm béo phì ở người có nguy cơ. BMI có thể đánh giá thấp mức độ thừa mỡ ở người già yếu và đánh giá cao ở vận động viên cơ bắp.
Vòng eo và tỉ lệ vòng eo chia cho chiều cao
Vòng eo và tỉ lệ vòng eo trên chiều cao là những chỉ số thiết thực để đánh giá phân bố mỡ. Tại Mỹ và Canada, ngưỡng vòng eo gợi ý nguy cơ tim mạch chuyển hóa là từ 102cm trở lên ở nam và 88cm trở lên ở nữ. Tại châu Âu, châu Phi, hạ Sahara và Trung Đông, các ngưỡng được đề xuất là 94cm ở nam và 80cm ở nữ. Tại Đông Á, Nam Á, Trung và Nam Mỹ, ngưỡng thường là 90cm ở nam và 80cm ở nữ.
Bằng chứng cho thấy, tỉ lệ vòng eo chia chiều cao là chỉ số vượt trội hơn số đo vòng eo trong dự đoán nguy cơ tim mạch. Ngưỡng từ 0,5 trở lên được xem là dấu hiệu tăng nguy cơ ở cả nam và nữ, phù hợp cho nhiều nhóm sắc tộc.
Những phương pháp đánh giá mỡ bổ sung như trở kháng điện, đo thể tích khí hoặc nước, chụp ba chiều hoặc DXA có thể hữu ích nếu BMI và thăm khám không rõ ràng hoặc cần làm sáng tỏ thêm. Dù cần thêm nghiên cứu để xác định ngưỡng chính xác tỉ lệ mỡ cơ thể trên 25% ở nam và trên 32% ở nữ có thể gợi ý nguy cơ tim mạch chuyển hóa liên quan béo phì.
Những phương pháp này đặc biệt quan trọng trong đánh giá người già yếu nghi ngờ giảm cơ kèm béo phì, người có BMI thấp nhưng mang biểu hiện bệnh liên quan béo phì và cũng hữu ích khi theo dõi khối cơ không mỡ hoặc thay đổi cơ xương trong quá trình giảm cân bằng thuốc hoặc phẫu thuật giảm cân. Hiện tại, giá trị ứng dụng lâm sàng còn hạn chế vì phụ thuộc vào chi phí, khả năng tiếp cận và chuẩn tham chiếu cần được tiếp tục củng cố bằng dữ liệu.
Thăm khám sau sàng lọc và đánh giá nhân trắc
Sau sàng lọc và đánh giá nhân trắc, người mắc béo phì cần được thăm khám toàn diện về những bệnh liên quan béo phì gồm khai thác bệnh sử tập trung vào béo phì, thăm khám và thực hiện xét nghiệm cần thiết.

Phân giai đoạn ABCD
Phân giai đoạn mức độ nặng về mặt lâm sàng của bệnh mạn tính do mô mỡ (ABCD) dựa trên sự hiện diện của những biến chứng liên quan béo phì (ORCD), từ đó quyết định cường độ điều trị. Như trình bày trong lưu đồ 4, AACE khuyến nghị một hệ thống phân giai đoạn đơn giản và phù hợp với thực hành lâm sàng:
- Giai đoạn 1: là khi người bệnh chưa có ORCD. Dù vậy, nhóm này vẫn có nguy cơ hình thành ORCD trong tương lai và cần được xem xét điều trị. Mục tiêu điều trị ở giai đoạn 1 là ngăn tăng cân và ngăn xuất hiện ORCD.
- Giai đoạn 2: là khi ORCD đã xuất hiện ở mức độ nhẹ đến trung bình.
- Giai đoạn 3: là khi có từ một biến chứng nặng trở lên. Mục tiêu điều trị ở giai đoạn 2 và 3 là phục hồi sức khỏe thông qua cải thiện hoặc đảo ngược ORCD đến mức mục tiêu. Mức độ giảm cân cần thiết để đạt được những mục tiêu này khác nhau, tùy vào loại ORCD và mức độ nặng.
Theo thuật ngữ được Ủy ban Lancet về béo phì khuyến nghị, giai đoạn 1 tương đương với béo phì tiền lâm sàng vì chưa có biến chứng rõ ràng, trong khi béo phì lâm sàng tương ứng với giai đoạn 2 hoặc 3, khi đã có ORCD. Giai đoạn 1 không có nghĩa là không cần điều trị. Giai đoạn này vẫn mang nguy cơ cao phát triển ORCD trong tương lai và cần được đề xuất điều trị dự phòng dựa trên quyết định chung.
Giai đoạn 1 mang nguy cơ tiến triển thành biến chứng xác định béo phì lâm sàng và nguy cơ tăng những bệnh liên quan như đái tháo đường típ 2 hoặc một số ung thư liên quan béo phì gồm đại tràng, thực quản, tuyến giáp, tủy xương, u lympho không Hodgkin, nội mạc tử cung và ung thư vú sau mãn kinh. AACE xem giai đoạn 1 là một phần của toàn bộ phổ bệnh ABCD.
Những hệ thống phân giai đoạn lâm sàng cho thấy, khả năng dự báo kết cục sức khỏe kể cả tử vong vượt trội so với chỉ số nhân trắc đơn thuần.
Hệ thống phân giai đoạn của AACE đánh giá sự hiện diện và mức độ nặng của nhiều ORCD có khả năng được dự phòng hoặc điều trị bằng giảm cân gồm tăng huyết áp, rối loạn lipid máu, rối loạn đường huyết từ tiền đái tháo đường đến nguy cơ đái tháo đường típ 2, đái tháo đường biểu hiện rõ hội chứng ngưng thở khi ngủ, rối loạn chức năng gan, hội chứng buồng trứng đa nang, thoái hóa khớp, bệnh tim mạch xơ vữa, suy tim, phân suất tống máu bảo tồn, bệnh thận mạn và các biến chứng khác.
Mức độ nặng của từng biến chứng được đánh giá dựa trên thăm khám xét nghiệm và triệu chứng của từng người.
Đánh giá lâm sàng
Người mắc ABCD cần được đánh giá bởi nhân viên y tế được đào tạo với định hướng chăm sóc tập trung biến chứng và có khả năng theo dõi dài hạn hoặc phối hợp chuyển tuyến khi cần. Việc đánh giá gồm bệnh sử liên quan cân nặng, các nỗ lực giảm cân trước đây, thăm khám toàn diện, đánh giá hệ cơ quan liên quan ABCD, khai thác gia đình, yếu tố xã hội, đánh giá thuốc đang dùng và xét nghiệm cần thiết để sàng lọc ORCD.
Những xét nghiệm được khuyến nghị để đánh giá nguy cơ chuyển hóa tim gồm creatinine để tính mức lọc cầu thận, lipid máu, đường huyết lúc đói, HbA1c và các chỉ số gan như AST, ALT và số lượng tiểu cầu nhằm tính chỉ số xơ hóa. Có thể làm thêm xét nghiệm tổng phân tích tế bào máu, điện giải, điện tim và xét nghiệm nước tiểu để đánh giá sức khỏe tổng quát.
Những xét nghiệm khác chỉ thực hiện khi thật sự cần, dựa trên bệnh sử, thăm khám và kết quả ban đầu nhằm đánh giá mức độ nặng của từng ORCD. Ví dụ như nghiệm pháp dung nạp glucose, hormone kích thích tuyến giáp, apolipoprotein B-100, cortisol, X-quang gối, siêu âm đàn hồi gan, đo đa ký giấc ngủ, xét nghiệm di truyền hoặc chuyển gửi tâm lý xã hội, dinh dưỡng.
AACE xem giai đoạn 2 và 3 áp dụng cho cả bệnh liên quan béo phì và biến chứng theo định nghĩa của Lancet. Về mặt thực hành, sự khác biệt giữa hai nhóm này không làm thay đổi hướng dẫn điều trị vì cả hai đều có thể cần điều trị giảm cân tùy theo mức độ nặng.
Người ở giai đoạn 1 cũng có thể cần điều trị dựa trên đánh giá lâm sàng và nguy cơ tiến triển. Điều trị vượt lên trên thay đổi hành vi và lối sống cần được cân nhắc ở mọi giai đoạn ABCD, khi mục tiêu là cải thiện sức khỏe.
Giai đoạn 2 và 3 của ABCD trong thuật toán AACE không tách biệt rõ ORCD vì cả bệnh và biến chứng đều có thể cải thiện bằng điều trị giảm cân. Sự phân biệt theo cách của Lancet đôi khi gây chồng lấn trong thực hành vì một biến chứng có thể mang tính chất của bệnh và ngược lại tùy theo cơ chế sinh lý bệnh.
Bảng 1. Ví dụ về ORCD có thể được phát hiện trong đánh giá lâm sàng ABCD

Xây dựng kế hoạch điều trị cá thể hóa
Việc xây dựng kế hoạch điều trị bắt đầu từ phân giai đoạn ABCD. Phương thức và cường độ điều trị cần phù hợp với giai đoạn lâm sàng phản ánh nguy cơ sự hiện diện và mức độ nặng của ORCD. Lựa chọn phương thức điều trị dựa trên mức độ giảm cân hoặc những lợi ích khác cần thiết để dự phòng hoặc cải thiện ORCD cụ thể. Điều trị có thể điều chỉnh nếu mức giảm cân không đủ để cải thiện chất lượng sống hoặc chưa giải quyết đầy đủ ORCD ảnh hưởng sức khỏe.
Người được điều trị cần tham gia vào quá trình xây dựng kế hoạch. Giá trị cá nhân, sở thích và khả năng tiếp cận dịch vụ cần được xem xét khi đặt mục tiêu điều trị, mục tiêu giảm cân và lựa chọn can thiệp lối sống, thuốc điều trị béo phì hoặc phẫu thuật giảm cân. Mục tiêu điều trị gồm giảm ổn định và duy trì cân nặng, đồng thời dự phòng giảm nhẹ và điều trị ORCD hướng đến sức khỏe tổng thể và chất lượng sống.
Để hỗ trợ kế hoạch cá thể hóa cần đánh giá các yếu tố sau:
- Béo phì khởi phát sớm trước 5 tuổi hoặc tình trạng ăn nhiều bất thường cần gợi ý xét nghiệm di truyền và tư vấn về khả năng mắc bệnh đơn gen hoặc hội chứng.
- Những nguyên nhân thứ phát gồm thuốc gây tăng cân, rối loạn nội tiết, hạn chế vận động và các bệnh lý khác.
- Thuốc điều trị bệnh đi kèm có khả năng gây tăng cân như insulin, sulfanylurea, một số thuốc chống loạn thần, thuốc chống trầm cảm, corticosteroid.
- Tác động của kỳ thị cân nặng và định kiến nội tại lên chất lượng sống và mức độ hợp tác điều trị.
- Sự hiện diện của rối loạn tâm lý như trầm cảm, lo âu hoặc rối loạn hành vi ăn uống.
- Yếu tố xã hội, khả năng hiểu biết sức khỏe và khả năng tiếp cận nguồn lực.
- Lý do tìm kiếm chăm sóc, mục tiêu điều trị, sở thích cá nhân, cũng như văn hóa trong lựa chọn chế độ ăn và vận động.
Theo dõi lâu dài
Người mắc bệnh mạn tính do mô mỡ mang một bệnh lý kéo dài suốt đời và cần được theo dõi dài hạn. Việc duy trì giảm cân đóng vai trò quan trọng để giữ được những lợi ích sức khỏe đã đạt được. Điều này rất khó trong thời gian dài vì sinh lý bệnh của quá trình thích nghi chuyển hóa gồm các cơ chế trung ương và ngoại biên thúc đẩy tăng cân trở lại, đồng thời biến chứng béo phì có thể nặng hơn hoặc tái phát.
Kế hoạch duy trì cân nặng cần được cá thể hóa nhằm xử lý yếu tố môi trường, hành vi và sinh lý thông qua theo dõi liên tục, hỗ trợ lối sống, điều trị y khoa và tái khám để giảm thiểu hậu quả sức khỏe bất lợi. Những điều chỉnh về lối sống và thay đổi thuốc điều trị béo phì có thể cần thiết ngay cả ở những người đã phẫu thuật chuyển hóa hoặc phẫu thuật giảm cân vì nhiều người vẫn tăng cân lại theo thời gian.
Cách tiếp cận điều trị để giảm cân ban đầu có thể khác với cách duy trì cân nặng ổn định lâu dài. Những thuốc điều trị béo phì với liều khác hoặc thấp hơn, miễn là dung nạp tốt, dễ tiếp cận và an toàn, đặc biệt với nguy cơ mất cơ và mất xương có thể mang lại lợi ích. Cần thêm nghiên cứu và phát triển thuốc để xác định chiến lược tối ưu cho điều trị dài hạn vừa hiệu quả, vừa an toàn.

Cá thể hóa mục tiêu giảm cân
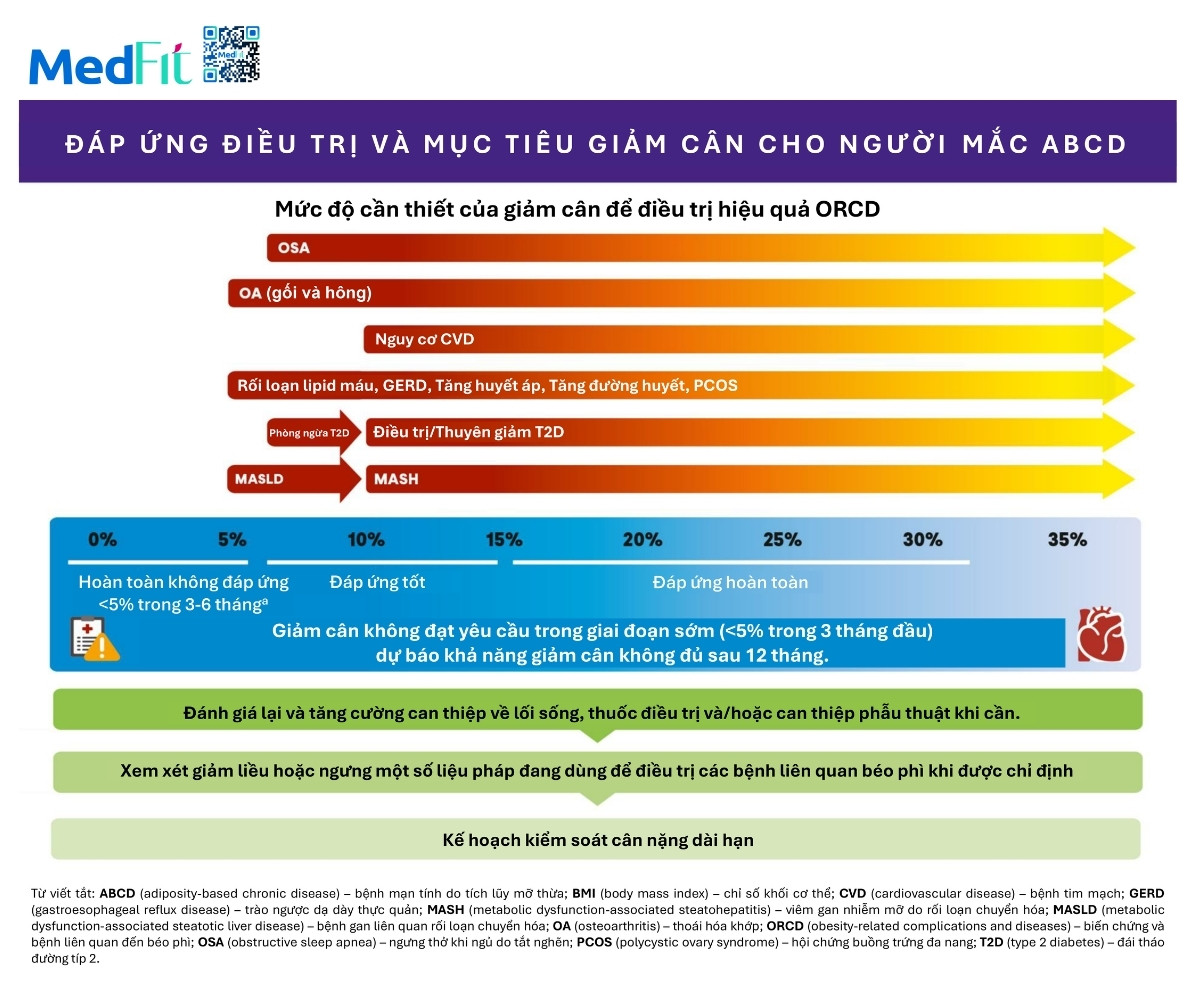
Lưu đồ 6 trình bày phạm vi mục tiêu giảm cân cần thiết để đạt được những kết quả sức khỏe mong muốn trong mô hình điều trị tập trung biến chứng. Mục tiêu giảm cân dựa trên mức giảm cân giúp cải thiện dự đoán được từng ORCD tồn tại ở mỗi người và có khả năng cải thiện khi giảm cân.
Bảng 2. Mục tiêu giảm cân liên quan đến lợi ích lâm sàng đối với các biến chứng của bệnh mạn tính do mô mỡ
| Biến chứng hoặc bệnh liên quan đến béo phì | Tỷ lệ giảm cân mang lại lợi ích lâm sàng có ý nghĩa | Tỷ lệ giảm cân giúp tăng thêm lợi ích |
| Phòng ngừa đái tháo đường típ 2 | 7%–10% (có thể thay đổi nếu thuốc có tác dụng kiểm soát đường huyết độc lập với giảm cân) | >10% (có thể thay đổi nếu thuốc có tác dụng kiểm soát đường huyết độc lập với giảm cân) |
| Thoái lui đái tháo đường típ 2 | 10% | >10% |
| Cải thiện tăng đường huyết | 5%–15% | >15% |
| Tăng huyết áp | 5%–15% | >15% |
| Rối loạn lipid máu | 5%–15% | >15% |
| Gan nhiễm mỡ | 5%–10% | >10% |
| MASH (viêm gan nhiễm mỡ do rối loạn chuyển hóa) | ≥10% (có thể thay đổi nếu thuốc có lợi ích độc lập với giảm cân) | ≥15% (có thể thay đổi nếu thuốc có lợi ích độc lập với giảm cân) |
| Ngưng thở khi ngủ do tắc nghẽn (OSA) | 7%–10% | >10% |
| Thoái hóa khớp (OA) | 5%–10% | >10% |
| Tiểu không kiểm soát do căng thẳng | 5%–10% | >10% |
| Trào ngược dạ dày thực quản (GERD) | 5%–10% | >10% |
| Hội chứng buồng trứng đa nang (PCOS) | 5%–15% | >15% |
| Phòng ngừa ung thư | Cần thêm nghiên cứu | |
| Bệnh tim mạch xơ vữa (ASCVD) và biến cố tim mạch lớn (MACE) | 10% (có thể thay đổi nếu thuốc có lợi ích độc lập với giảm cân) | >10% (có thể thay đổi nếu thuốc có tác dụng kiểm soát đường huyết độc lập với giảm cân) |
Lưu đồ 6 và bảng 2 cho thấy, từng loại ORCD đòi hỏi mức giảm cân khác nhau. Tỉ lệ phần trăm giảm cân được xem như một dạng dấu ấn sinh học có thể nhắm đến nhằm đảm bảo mức giảm cân đủ để cải thiện ORCD được theo dõi bằng thăm khám lâm sàng, dữ liệu xét nghiệm như huyết áp, đường máu, HbA1c, lipid, đo chức năng và triệu chứng người bệnh báo cáo.
Mức giảm cân và đáp ứng điều trị được đánh giá cả về mặt nhân trắc và lâm sàng để quyết định bước tiếp theo. Sức khỏe của người bệnh chi phối cuộc trao đổi, quyết định điều trị chung gồm tăng cường hoặc giảm cường độ điều trị.
Nhóm chuyên gia đề xuất 3 mức giảm cân liên quan tới lợi ích sức khỏe gồm:
- Giảm ≤ 5% được xem là đáp ứng chưa đầy đủ vì thường không đủ để điều trị biến chứng.
- Giảm 5-10% được xem là đáp ứng tốt và có thể hoặc không tối ưu cho một số biến chứng.
- Giảm từ 15% trở lên được xem là đáp ứng xuất sắc vì đủ để điều trị hoặc dự phòng nhiều ORCD.
Dù vậy, mức độ cải thiện biến chứng và mức giảm cân thu được khác nhau giữa từng người. Mục tiêu luôn là đạt mức giảm cân đủ để cải thiện sức khỏe mỗi người.
Hiệu quả điều trị bằng thuốc giảm cân cần được đánh giá sau khoảng 3 tháng dùng liều điều trị. Nếu giảm cân không đạt ít nhất 5%, khả năng hiệu quả dài hạn sẽ hạn chế và cần thay đổi cách điều trị bằng cách tăng cường điều chỉnh lối sống, đổi thuốc điều trị béo phì hoặc phối hợp thuốc.
Những người đạt giảm cân từ 5% trở lên có thể tiếp tục với điều trị hiện tại. Khi theo dõi lâu dài, nếu mục tiêu cải thiện ORCD chưa đạt có thể cần tăng cường điều trị. Cường độ điều trị khi khởi đầu và theo dõi lâu dài cần tương ứng với mức độ nặng hoặc giai đoạn ABCD.
Những người giảm từ 15% trở lên, tương ứng mức giảm cân trung bình đạt được bằng thuốc thế hệ 2 sẽ nhận được lợi ích dự đoán rõ rệt trong phòng và trị nhiều ORCD. Khi lựa chọn thuốc giảm cân để đạt mục tiêu cá thể hóa, cần cân nhắc hiệu quả giảm cân của từng thuốc. Việc này gặp khó khăn vì thiếu các nghiên cứu so sánh trực tiếp. Trong các thử nghiệm giai đoạn 3, những thuốc thế hệ 1 được phê duyệt trước năm 2014 thường cho mức giảm cân dưới 10% gồm orlistat, naltrexone-bupropion, liraglutide và phentermine-topiramate trong đó phentermine-topiramate có hiệu quả cao nhất gần 10%.
Thuốc thế hệ 2 như semaglutide và tirzepatide đạt mức giảm trung bình từ 15% trở lên. Thuốc setmelanotide đạt mức giảm tương tự ở người mắc béo phì đơn gen. Hiện đã có bằng chứng để xây dựng hệ thống phân cấp thuốc, ưu tiên trong điều trị tập trung biến chứng dựa trên sự hiện diện của từng ORCD.
Duy trì giảm cân giữ vai trò quan trọng trong duy trì lợi ích sức khỏe. ORCD sẽ nặng hơn khi tăng cân trở lại. Giảm cường độ điều trị những bệnh như đái tháo đường típ 2, tăng huyết áp hoặc rối loạn lipid máu có thể bắt đầu sau khi đạt mức giảm cân ban đầu, tuy vậy cần theo dõi sát và điều chỉnh thuốc khi cần.
Phẫu thuật chuyển hóa và phẫu thuật dạ dày giảm cân
Những phẫu thuật như cắt dạ dày kiểu tay áo, phẫu thuật Roux-en-Y và phẫu thuật một nối vị tràng đã được chứng minh hiệu quả cao trong giảm cân và cải thiện sức khỏe cho người mắc ABCD, đặc biệt khi BMI từ 40 trở lên hoặc BMI từ 35 trở lên kèm ORCD. Hiện những phẫu thuật phổ biến nhất là cắt dạ dày tay áo và Roux-en-Y chiếm khoảng 90% toàn cầu với dữ liệu an toàn trung và dài hạn được ghi nhận rõ.
Những phẫu thuật khác gồm chuyển dạng mật tụy với nối tắt tá tràng, phẫu thuật một nối vị tràng và đặt vòng dạ dày điều chỉnh, tuy vậy hiệu quả dài hạn của đặt vòng dạ dày kém nên ít dùng. Đa số phẫu thuật hiện nay được thực hiện qua đường mổ ít xâm lấn như nội soi hoặc robot hỗ trợ. Những phương pháp can thiệp nội soi ngắn hạn như bóng dạ dày ít hiệu quả hơn và thiếu bằng chứng lợi ích dài hạn. Dù vậy các thiết bị nội soi có thể được cân nhắc như biện pháp bổ trợ kết hợp thuốc điều trị béo phì.
Ngưỡng BMI để cân nhắc phẫu thuật từ lâu là 40kg/m2 hoặc từ 35kg/m2 trở lên kèm ORCD. Năm 2016, 45 hiệp hội chuyên môn quốc tế cùng khuyến cáo phẫu thuật chuyển hóa cho người mắc đái tháo đường típ 2 và BMI từ 30-34,9kg/m2 khi đường huyết không kiểm soát dù đã tối ưu điều trị bằng thuốc uống hoặc thuốc tiêm.
Hiện Hiệp hội Phẫu thuật Chuyển hóa và Giảm cân Hoa Kỳ cùng Liên đoàn Quốc tế về Phẫu thuật Béo phì khuyến nghị phẫu thuật cho người trưởng thành có BMI từ 35kg/m2 trở lên bất kể mức độ nặng của bệnh liên quan béo phì, đồng thời cho người có BMI từ 30-34,9kg/m2 kèm bệnh tim mạch chuyển hóa nặng như đái tháo đường típ 2 và bệnh tim mạch.
Những can thiệp hiệu quả cao này cần được kết hợp với dinh dưỡng, vận động và trị liệu hành vi cùng khả năng sử dụng thuốc điều trị béo phì trước hoặc sau phẫu thuật khi cần. Mô hình chăm sóc đa chuyên khoa cho giai đoạn quanh phẫu thuật và theo dõi lâu dài là bắt buộc để đạt kết quả tối ưu.

Can thiệp lối sống
Ngoài thuốc điều trị béo phì và phẫu thuật, những can thiệp lối sống luôn giữ vai trò nền tảng để tối ưu kết quả sức khỏe ở người mắc ABCD. Lưu đồ 7 trình bày những biện pháp không dùng thuốc gồm dinh dưỡng, hoạt động thể lực, giấc ngủ, giảm căng thẳng và trị liệu hành vi cá thể hóa.
Dinh dưỡng
Dinh dưỡng và lượng năng lượng nạp vào là yếu tố then chốt trong điều hòa cân bằng năng lượng nên ảnh hưởng trực tiếp đến mức độ tích lũy mỡ. Việc chỉ tập trung vào khẩu hiệu “calo nạp vào, calo tiêu hao” dễ làm đơn giản hóa quá mức sinh lý bệnh phức tạp của béo phì và vô tình làm tăng kỳ thị.
Giảm cân chắc chắn cần tạo chênh lệch năng lượng theo hướng sử dụng nhiều năng lượng dự trữ hơn năng lượng được cung cấp qua ăn uống, tuy vậy chất lượng khẩu phần với đủ các nhóm đa lượng và vi lượng vẫn rất quan trọng vì giúp duy trì khối cơ và khối xương đồng thời nâng đỡ sức khỏe tổng thể.
Can thiệp dinh dưỡng nên tập trung vào chất lượng và mật độ dinh dưỡng của thực phẩm, hạn chế tối đa thực phẩm siêu chế biến và giàu năng lượng trong bối cảnh phù hợp với chuẩn mực tâm lý xã hội và văn hóa. Can thiệp dinh dưỡng phải tạo được mức thâm hụt năng lượng để giảm cân nhưng rất khó duy trì lâu dài nếu thiếu hỗ trợ bằng thuốc hoặc phẫu thuật. Dù tuân thủ các hướng dẫn ăn uống, nhiều người vẫn tăng cân trở lại do những đáp ứng thích nghi bất lợi sau giảm cân, vốn là một phần của sinh lý bệnh béo phì.
Việc tạo thâm hụt năng lượng để giảm cân có thể đạt được bằng nhiều chiến lược dinh dưỡng dựa trên bằng chứng, có thể kết hợp hoặc điều chỉnh linh hoạt theo từng cá nhân. Mô hình ăn uống nên được tối ưu không chỉ để giảm cân mà còn hướng tới các lợi ích sức khỏe rộng hơn, đồng thời phản ánh sở thích cá nhân, bối cảnh văn hóa, mục tiêu sức khỏe và khả năng tiếp cận thực phẩm.
Cần chú ý đặc biệt đến chất lượng khẩu phần ở những người đang giảm cân mạnh, ví dụ dùng thuốc điều trị béo phì thế hệ 2, để bảo đảm cung cấp đủ protein, chất xơ, sắt, canxi và những vi chất khác.

Can thiệp dinh dưỡng
Người thừa cân hoặc béo phì cần được tư vấn và hỗ trợ để xây dựng kế hoạch dinh dưỡng cá thể hóa, vẫn tôn trọng quyền tự chủ và sở thích văn hóa trong ăn uống nhưng đồng thời phù hợp với mục tiêu cân nặng và sức khỏe. Có rất nhiều mô hình thực đơn với tỉ lệ các chất đa lượng khác nhau có thể được áp dụng dưới dạng khẩu phần giảm năng lượng nhằm hỗ trợ giảm cân an toàn và cải thiện sức khỏe.
Khi thay đổi lối sống là biện pháp điều trị chính, các khuyến nghị thường đề xuất khẩu phần thiếu hụt khoảng 500-750kcal/ngày hoặc ước tính tổng năng lượng khoảng 1200-1500kcal/ngày cho phụ nữ và nam giới tương ứng, dựa trên mức tiêu hao năng lượng nền được tính lúc ban đầu bằng các công cụ như máy tính của Viện Y tế Quốc gia Hoa Kỳ.
Trong số các kiểu thực đơn phổ biến như Địa Trung Hải, DASH, chế độ giàu carbohydrate phức, ít carbohydrate, ăn chay hoặc nguồn gốc thực vật, kiểu “paleo” và những mô hình khác, chưa có tỉ lệ các chất đa lượng nào được chứng minh vượt trội tuyệt đối. Yếu tố quan trọng hơn chính là khả năng tuân thủ lâu dài.
Dữ liệu an toàn vượt quá 2-3 năm còn hạn chế với nhiều mô hình và đến hiện tại, lợi ích giảm nguy cơ tim mạch dài hạn mới chỉ được chứng minh rõ với chế độ ăn Địa Trung Hải. Kế hoạch thay thế bữa ăn và các chiến lược về thời điểm ăn hoặc nhịn ăn gián đoạn có thể được phối hợp cùng những can thiệp dinh dưỡng cá thể hóa khác.
Trong giai đoạn tăng liều thuốc điều trị béo phì và thời kì ăn giảm năng lượng tích cực, việc bảo đảm đủ dinh dưỡng và áp dụng thực hành ăn uống giúp giảm tác dụng phụ là rất quan trọng. Với tác dụng ức chế thèm ăn mạnh của thuốc thế hệ 2, trọng tâm không chỉ ở việc cắt giảm năng lượng mà chuyển sang bảo đảm chất lượng khẩu phần.
Một số điểm định hướng quan trọng gồm:
- Ưu tiên các nguồn carbohydrate giàu dinh dưỡng như rau, các loại đậu và trái cây.
- Ưu tiên nguồn đạm ít béo.
- Cân nhắc bổ sung đa vitamin có chứa sắt và canxi.
- Linh hoạt sử dụng sản phẩm thay thế bữa ăn khi phù hợp.
Để giảm tác dụng phụ trên đường tiêu hóa của nhóm thuốc chủ vận đồng thể GLP-1 một và các thuốc điều trị béo phì khác, có thể tư vấn người bệnh:
- Ăn chậm để giảm khó chịu liên quan thuốc.
- Ăn thành nhiều bữa nhỏ trong ngày.
- Giảm thức ăn nhiều chất béo hoặc những món dễ làm nặng triệu chứng.
- Ghi nhận những thực phẩm làm tăng khó chịu đường tiêu hóa để điều chỉnh.
- Duy trì uống đủ nước.
Protein là chất đa lượng then chốt cần ưu tiên trong giai đoạn giảm cân để hạn chế mất khối cơ. Trước đây, người ta lo ngại khẩu phần giàu đạm có thể làm xấu đi bệnh thận mạn nhưng việc hạn chế đạm dưới 0,85g/kg chưa được chứng minh làm chậm suy thận. Hướng dẫn gần đây gợi ý giữ lượng protein từ 1,2g/kg trở lên cho đa số người trưởng thành và từ 0,8g/kg trở lên cho người mắc đái tháo đường kèm bệnh thận mạn chưa lọc máu.
Lượng protein cao hơn, từ 2,3g/kg trở lên, có thể cần thiết để tối ưu bảo tồn khối nạc trong bối cảnh đang ưu tiên tập luyện kháng lực trong thời kỳ ăn giảm năng lượng. Khẩu phần đạm rất cao trên 2g/kg trong thời gian dài có thể không gây hại nhưng ngưỡng giới hạn cao nhất được cho là khoảng 3,5g/kg/ngày.
Hoạt động thể chất
Hoạt động thể chất bao gồm vận động aerobic, tập kháng lực hoặc tăng sức mạnh, giảm thời gian ngồi một chỗ và gia tăng các hình thức vận động ngoài giờ tập chính thức. Đây là một phần quan trọng trong điều trị người thừa cân hoặc béo phì để cải thiện sức khỏe tổng quát. Nhiều khuyến cáo về béo phì và các biến chứng như đái tháo đường típ 2 đều nhấn mạnh vai trò của kê đơn vận động trong điều trị.
AACE khuyến nghị kê đơn vận động cá thể hóa phù hợp với sở thích và khả năng của từng người. Mục tiêu thường hướng tới là khoảng 150 phút/tuần hoạt động aerobic cường độ trung bình, chia trên ít nhất 3 ngày. Tập kháng lực toàn thân từ 2-3 buổi/tuần được khuyến khích và nên được ưu tiên đặc biệt khi giảm cân bằng thuốc hoặc phẫu thuật với mục tiêu duy trì hay cải thiện khối cơ nạc.
Để duy trì cân nặng sau giai đoạn giảm cân bằng thay đổi hành vi, điều trị y khoa hoặc can thiệp phẫu thuật, thường cần mức vận động cao hơn, khoảng 200-300 phút/tuần hoạt động aerobic cường độ trung bình, vẫn đặt ưu tiên cho bài tập kháng lực nhằm bảo tồn khối cơ. Việc giữ khối cơ thông qua tập kháng lực trong giai đoạn giảm cân giúp duy trì chuyển hóa cơ bản và tổng chi tiêu năng lượng.
Người lớn tuổi hoặc những người có nguy cơ yếu cơ đặc biệt là nhóm giảm cơ kèm béo phì càng cần chú trọng tập kháng lực kết hợp khẩu phần đủ protein vì mất khối cơ ở nhóm này gây hại lớn về mặt chuyển hóa, chức năng vận động và làm tăng nguy cơ té ngã hoặc gãy xương.
Các mục tiêu vận động được nêu trong khuyến cáo thường không dễ đạt được ngay từ đầu đối với người béo phì. Do đó kê đơn vận động cần được cá thể hóa, xuất phát từ khả năng hiện tại của từng người. Có thể áp dụng hai nguyên tắc thực hành dễ nhớ là bắt đầu ở cường độ thấp và tăng dần tùy sức và bất kỳ mức vận động nào cũng tốt hơn không vận động.
Với người ít kinh nghiệm tập luyện hoặc có hạn chế vận động, việc bắt đầu một chương trình tập phù hợp và an toàn có thể là thách thức. Một cách tiếp cận rất thực tế là khuyến khích những đợt vận động ngắn và dễ thực hiện, chẳng hạn đi bộ một quãng ngắn giờ nghỉ trưa hoặc tập đứng dậy đi lại thường xuyên hơn trong ngày.
Những bài tập tại ghế, tập dưới nước và hỗ trợ từ chuyên viên vật lý trị liệu có thể giúp người hạn chế chức năng tìm được các bài tập an toàn. Khi có điều kiện, các chương trình thể dục y khoa hỗ trợ tốt cho người mới bắt đầu tiếp cận tập kháng lực và nhiều dạng bài tập khác.

Giấc ngủ
Ngủ không đủ thời gian dưới 7-8 giờ/đêm và chất lượng giấc ngủ kém có thể dẫn đến rối loạn kiểm soát ăn uống, thay đổi chuyển hóa và tăng nguy cơ béo phì. Thiếu ngủ và rối loạn nhịp sinh học liên quan đến tăng cảm giác đói, tăng lượng năng lượng nạp vào, giảm tiêu hao năng lượng và tăng nguy cơ bệnh tim mạch chuyển hóa.
Với người có thời gian ngủ ngắn có thể tư vấn vệ sinh giấc ngủ một cách cá thể hóa nhằm kéo dài thời lượng ngủ, qua đó giúp giảm lượng thức ăn nạp vào và hỗ trợ giảm cân. Hội chứng ngưng thở khi ngủ tắc nghẽn là một biến chứng rất thường gặp của béo phì nhưng thường bị bỏ sót và không được điều trị. Mối liên hệ sinh lý bệnh giữa ngưng thở khi ngủ và béo phì phức tạp, hai tình trạng này cùng gắn với kháng insulin và tăng nguy cơ tim mạch.
Trong nghiên cứu Sleep AHEAD, chương trình can thiệp lối sống giúp giảm cân đã cải thiện rõ rệt ngưng thở khi ngủ và chỉ số ngưng thở giảm thở ở người béo phì mắc đái tháo đường típ 2. Điều trị ngưng thở khi ngủ bằng áp lực dương liên tục đường thở đơn thuần dường như không giúp tăng hiệu quả giảm cân.
Vì vậy, giấc ngủ là một trụ cột quan trọng trong phòng ngừa và quản lý béo phì cùng các bệnh liên quan. Người thừa cân hoặc béo phì cần được tư vấn về tầm quan trọng của ngủ đủ và giữ nhịp sinh học lành mạnh. Cần sàng lọc ngưng thở khi ngủ ở những người có triệu chứng điển hình, vòng cổ lớn > 17inch ở nam, > 16inch ở nữ hoặc có nguy cơ cao mắc hội chứng này.
Thành kiến cân nặng, kỳ thị, rối loạn tâm lý và trị liệu hành vi
Thành kiến cân nặng được hiểu là những quan điểm tiêu cực hướng vào người đang sống chung với béo phì, còn kỳ thị cân nặng là những suy nghĩ và hành vi phân biệt đối xử nhắm đến người béo phì xuất phát từ thành kiến này. Hai hình thức giao tiếp bằng lời và không lời thể hiện kỳ thị đều ảnh hưởng đến quá trình chăm sóc y khoa và cho thấy sự tồn tại của những rào cản mang tính hệ thống trong tiếp cận chăm sóc sức khỏe.
Thành kiến và kỳ thị cân nặng có thể dẫn đến sự nội tâm hóa thành kiến, khi người béo phì tự gán những định kiến tiêu cực vào bản thân và rơi vào tự hạ thấp giá trị. Sự nội tâm hóa này tác động xấu đến sức khỏe thể chất và tinh thần, làm giảm chất lượng sống liên quan sức khỏe và khiến việc tuân thủ điều trị gặp khó khăn. Mức độ nội tâm hóa thành kiến tỉ lệ nghịch với động lực duy trì lối sống lành mạnh và góp phần dẫn đến những kết quả sức khỏe bất lợi.
Vì những lý do này, AACE là tổ chức đầu tiên khuyến nghị xem xét sự nội tâm hóa thành kiến cân nặng trong quá trình đánh giá và phân giai đoạn người béo phì, đồng thời đưa nội dung này vào kế hoạch điều trị cá thể hóa.
Bảng câu hỏi Kỳ thị cân nặng tự thân và Thang đo Nội tâm hóa thành kiến cân nặng là những công cụ đã được kiểm chứng giá trị nhằm đánh giá tình trạng này trong thực hành lâm sàng. Nội tâm hóa thành kiến cân nặng là yếu tố dự báo mạnh nhất cho căng thẳng lo âu trầm cảm và sự không hài lòng với hình thể.
Cách tiếp cận lấy người bệnh làm trung tâm trong giao tiếp liên quan cân nặng cần sử dụng ngôn ngữ ưu tiên con người và bày tỏ sự thấu cảm khi đề cập tới vấn đề sức khỏe. Người bệnh nên được cung cấp toàn bộ lựa chọn điều trị dựa trên bằng chứng gồm can thiệp lối sống thuốc điều trị béo phì và các can thiệp phẫu thuật. Nhân viên y tế cần trình bày rõ lợi ích và nguy cơ với cách diễn đạt phù hợp mức hiểu biết sức khỏe của từng người.
Liệu pháp nhận thức hành vi có thể hỗ trợ người béo phì duy trì những lựa chọn lối sống lành mạnh bằng cách thúc đẩy thay đổi về nhận thức theo hướng hỗ trợ giảm cân và tối ưu hóa sức khỏe.
Nhân viên y tế cần chú ý đến khía cạnh tâm lý gắn với tình trạng thừa cân hoặc béo phì và khả năng xuất hiện rối loạn tâm lý ở người mắc bệnh mạn tính do mô mỡ. Trầm cảm lo âu và rối loạn ăn uống theo kiểu ăn uống vô độ phổ biến hơn ở người béo phì so với cộng đồng. Những vấn đề này có thể cần được can thiệp sớm để đảm bảo kế hoạch điều trị đạt hiệu quả.
Việc chuyển gửi sang chuyên gia tâm lý để sàng lọc tâm lý và trị liệu nhận thức hành vi nên được xem xét như một phần của theo dõi dài hạn ở người có nội tâm hóa thành kiến cân nặng. Sự phối hợp với chuyên gia tâm lý thông qua chuyển gửi hoặc trong mô hình đội ngũ đa chuyên khoa giúp mang lại chăm sóc toàn diện hơn cho người mắc ABCD.
Lưu đồ 10 cung cấp hướng dẫn hỗ trợ Bác sĩ trong cá thể hóa điều trị dựa trên mô hình điều trị tập trung biến chứng nhằm hướng đến từng ORCD cụ thể. Hệ thống phân cấp thuốc ưu tiên được đề xuất dựa trên dữ liệu từ các thử nghiệm lâm sàng. Những phân cấp này được củng cố bởi các thử nghiệm giai đoạn 3 đã đánh giá khả năng thuốc điều trị béo phì can thiệp vào ORCD như một tiêu chí chính hoặc tiêu chí được chỉ định trước. Điều này không phủ nhận khả năng giảm cân dù bằng phương pháp nào vẫn mang lại lợi ích như mô tả trong lưu đồ 7.

Các ORCD chuyển hóa tim mạch (cardiometabolic ORCD)
Các ORCD chuyển hóa tim mạch là nhóm biến chứng ảnh hưởng trực tiếp đến hệ tim mạch và chuyển hóa, đóng vai trò quan trọng trong đánh giá và điều trị ABCD.
Tiền đái tháo đường, hội chứng chuyển hóa và dự phòng đái tháo đường
- Semaglutide hoặc tirzepatide: được ưu tiên hàng đầu để ngăn tiến triển sang đái tháo đường thật sự vì mang lại giảm cân rất lớn đồng thời có tác dụng trực tiếp trên đường huyết nhờ cơ chế incretin và còn đem lại nhiều lợi ích tim mạch chuyển hóa quan trọng khác như cải thiện lipid huyết áp và tình trạng viêm.
- Liraglutide và phentermine-topiramate: được xếp nhóm thuốc hàng 2 nhưng vẫn rất hiệu quả trong mục tiêu này.
- Orlistat: được xem là lựa chọn hàng 3.
Đái tháo đường típ 2 (T2D)
- Tirzepatide hoặc semaglutide: là thuốc hàng đầu trong điều trị người mắc đái tháo đường típ 2 có béo phì dựa trên mức giảm cân đạt được khả năng hạ HbA1c về mục tiêu và tỷ lệ hạ đường huyết thấp.
- Liraglutide và phentermine-topiramate: là thuốc hàng 2 nhưng vẫn có hiệu quả tốt.
- Orlistat và naltrexone kết hợp bupropion: được xếp nhóm thuốc hàng 3.
Dự phòng biến cố tim mạch bất lợi chính (MACE)
- Semaglutide: cho đến hiện tại, semaglutide là thuốc điều trị béo phì duy nhất đã chứng minh giảm nguy cơ MACE trong thử nghiệm kết cục tim mạch trên người béo phì chưa mắc đái tháo đường (dự phòng thứ phát).
- Tirzepatide: có thể cũng mang lại lợi ích bảo vệ tim dựa trên phân tích hậu kiểm từ nhánh mở rộng của thử nghiệm SURMOUNT-1 cho thấy tỉ số nguy cơ đối với MACE giảm.
- Liraglutide: liều 1,8mg/ngày chứng minh được hiệu quả bảo vệ tim ở người béo phì mắc đái tháo đường típ 2 trong thử nghiệm LEADER.
- Tirzepatide: một thử nghiệm về tỷ lệ mắc bệnh và tử vong do tim mạch với tirzepatide đang diễn ra.
- Orlistat, naltrexone-bupropion và phentermine-topiramate: chưa có dữ liệu kết luận lợi ích tim mạch.
Viêm gan nhiễm mỡ tiến triển do rối loạn chuyển hóa (MASH)
Semaglutide và tirzepatide là các thuốc ưu tiên trong điều trị MASH dựa trên dữ liệu cho thấy cải thiện mô bệnh học gan và xơ hóa. Bất kỳ can thiệp giảm cân nào đạt được mức giảm từ 5-10% cân nặng hoặc hơn đều được dự đoán sẽ làm giảm mỡ gan.
Tăng huyết áp
- Tirzepatide và semaglutide, sau đó là phentermine-topiramate dạng giải phóng kéo dài: được ưu tiên cho người mắc ABCD kèm tăng huyết áp dựa trên các cải thiện huyết áp ghi nhận trong thử nghiệm lâm sàng.
- Liraglutide và orlistat: được xếp vào nhóm thuốc hàng 2.
Bệnh thận mạn (CKD)
- Semaglutide: là thuốc ưu tiên trong điều trị bệnh thận mạn dựa trên dữ liệu thử nghiệm ở người đái tháo đường típ 2 cho thấy liều 1mg/tuần giúp làm chậm tốc độ suy giảm mức lọc cầu thận ước tính và giảm biến cố thận.
- Liraglutide: liều 1,8mg/ngày ở người đái tháo đường típ 2 cũng cho thấy hiệu quả bảo vệ thận trong phân tích thứ cấp của thử nghiệm LEADER.
- Tirzepatide: một thử nghiệm đánh giá tác động của tirzepatide lên chức năng thận đang tiến hành và phân tích hậu kiểm trước đó ở người đái tháo đường típ 2 cũng ủng hộ kỳ vọng tirzepatide sẽ cho kết quả tích cực.
Suy tim với phân suất tống máu bảo tồn (HFpEF)
- Tirzepatide: đã được chứng minh giúp cải thiện triệu chứng chức năng thể lực và các kết cục liên quan suy tim như nhu cầu khám cấp cứu hoặc nhập viện ở người mắc HFpEF.
- Semaglutide: cũng cho thấy hiệu quả cải thiện triệu chứng và khả năng gắng sức ở nhóm này.
Các ORCD cơ học (biomechanical ORCD)
Các ORCD cơ học là nhóm biến chứng xuất hiện khi trọng lượng dư thừa tạo áp lực lên cấu trúc cơ xương khớp và ảnh hưởng đến khả năng vận động hằng ngày.
Thoái hóa khớp (OA)
Semaglutide là thuốc ưu tiên cho người béo phì kèm thoái hóa khớp gối dựa trên dữ liệu thử nghiệm lâm sàng. Giảm hơn 5% cân nặng có thể cải thiện triệu chứng thoái hóa khớp.
Ngưng thở khi ngủ tắc nghẽn (OSA)
Tirzepatide và phentermine/topiramate là những thuốc ưu tiên trong điều trị OSA ở người ABCD dựa trên dữ liệu cho thấy giảm triệu chứng và cải thiện chỉ số ngưng thở giảm thở trên đa ký giấc ngủ. Tirzepatide hiện đã được FDA Hoa Kỳ phê duyệt để điều trị OSA mức độ vừa và nặng ở người trưởng thành béo phì.
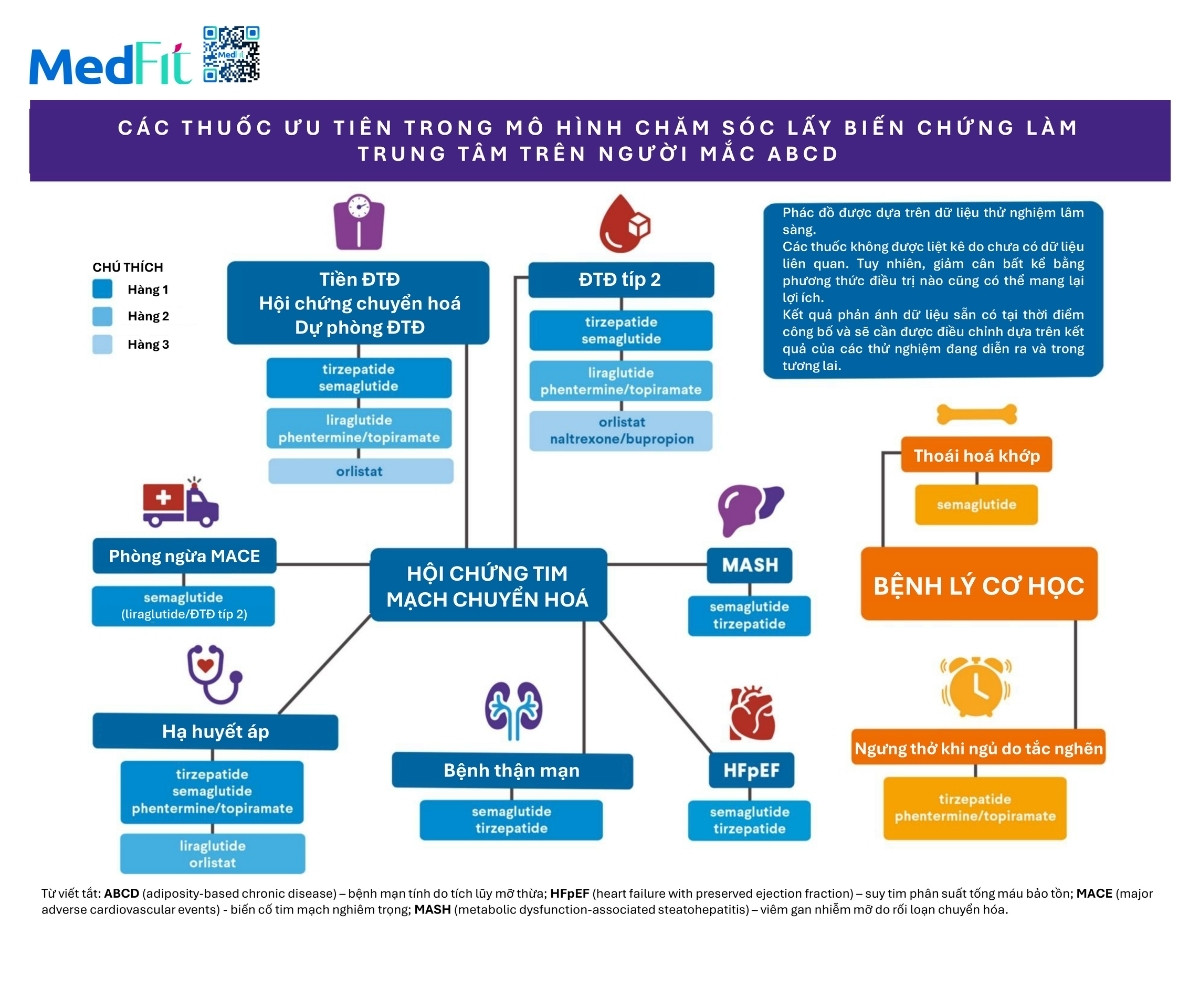
Thuốc điều trị béo phì
Bác sĩ cần cân nhắc đồng thời hai nhóm lợi ích của thuốc điều trị béo phì gồm hiệu quả giảm cân và khả năng cải thiện những biến chứng hay bệnh đi kèm không hoàn toàn do béo phì. Đồng thời cần tính đến tác dụng phụ đã biết và chi phí thuốc. Khi chi phí và mức chi trả của bảo hiểm là rào cản có thể cân nhắc sử dụng thuốc gốc dùng ngoài chỉ định nếu có bằng chứng hỗ trợ hiệu quả điều trị.
Ngoài tác dụng giảm các ORCD cụ thể, topiramate, phentermine/topiramate, liraglutide và semaglutide đã cho thấy khả năng giảm ăn vô độ hoặc thèm ăn mạnh, với naltrexone/bupropion có xu hướng mang lại lợi ích nhưng kết quả còn không đồng nhất. Một số chỉ định khác cần lưu tâm gồm topiramate trong điều trị đau nửa đầu, naltrexone và các thuốc đồng vận GLP-1 trong điều trị lệ thuộc rượu và bupropion trong hỗ trợ cai thuốc lá.
Việc dùng thuốc để xử trí tăng cân trở lại hoặc để đạt mục tiêu lâm sàng sau phẫu thuật chuyển hóa giảm cân chưa được bàn sâu trong tài liệu này, tuy vậy thuốc điều trị béo phì có thể là công cụ hữu ích hỗ trợ người bệnh sau mổ.
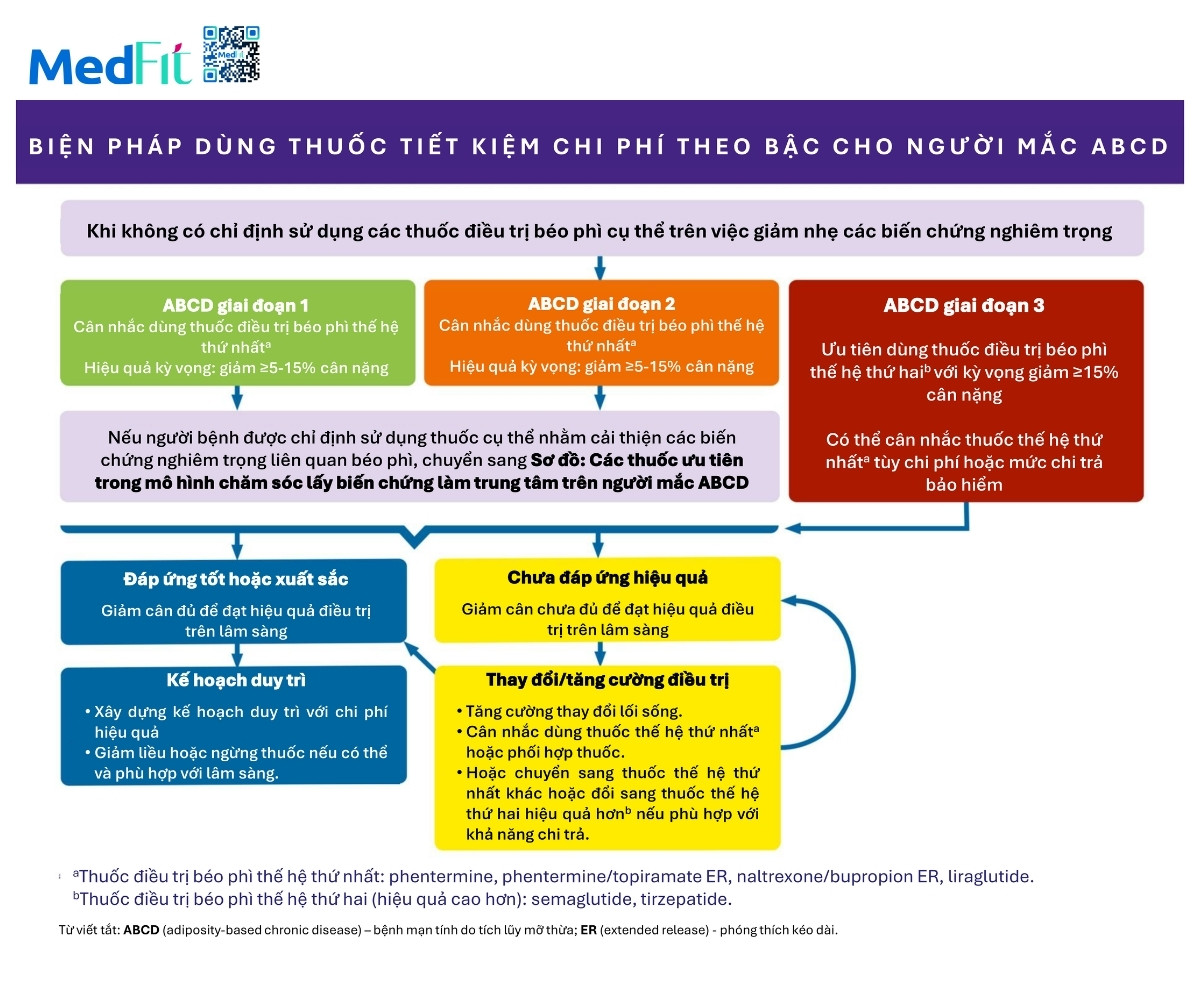
Thuốc điều trị béo phì thế hệ 2 có chi phí rất cao, đặc biệt tại Hoa Kỳ và nhiều người không có bảo hiểm chi trả nên khó tiếp cận dù đây là các liệu pháp dựa trên bằng chứng. Vì thế, cần nhớ rằng các thuốc thế hệ 1 như phentermine, orlistat, phentermine/topiramate, naltrexone/bupropion và liraglutide vẫn có thể được sử dụng hiệu quả để giảm cân và điều trị nhiều ORCD ở phần lớn người bệnh.
Những thuốc này ít tốn kém hơn, dễ tiếp cận hơn và có thể cân nhắc cho người ở giai đoạn 1 hoặc 2 của ABCD, trong khi thuốc thế hệ 2 nên được ưu tiên sử dụng khi có thể cho bệnh giai đoạn 3 nếu cần mức giảm cân lớn để xử trí biến chứng nặng hơn.
Thuốc thế hệ 1 đã được chứng minh trong các thử nghiệm lâm sàng là có khả năng cải thiện một số biến chứng của béo phì và có thể được dùng để cải thiện huyết áp, mỡ máu, gan nhiễm mỡ, dự phòng đái tháo đường (liraglutide và phentermine/topiramate), điều trị OSA (phentermine/topiramate), điều trị đái tháo đường típ 2 (tất cả thuốc thế hệ 1) và bảo vệ tim thận ở người đái tháo đường típ 2 (liraglutide).
Nếu mức giảm cân chưa đủ để đạt mục tiêu lâm sàng có thể cân nhắc đổi sang thuốc thế hệ 1 khác, tăng cường can thiệp lối sống hoặc chuyển sang thuốc thế hệ 2. Sức khỏe của từng người mới là trọng tâm thông qua việc đạt mục tiêu lâm sàng trong mô hình điều trị tập trung biến chứng. Các biến chứng và bệnh liên quan cũng có thể cần các điều trị đặc hiệu không liên quan đến giảm cân song song.
Ngoài ra, có thể cân nhắc dùng thuốc thế hệ 1 để duy trì cân nặng sau khi đã giảm bằng thuốc thế hệ 2 như một chiến lược có chi phí và khả năng tiếp cận tốt hơn cho giai đoạn duy trì.
Cá thể hóa lựa chọn thuốc và các sơ đồ điều trị
Lưu đồ 10 cung cấp hướng dẫn giúp cá thể hóa lựa chọn thuốc điều trị béo phì dựa trên ORCD, bệnh đi kèm và nguy cơ tác dụng phụ mặc dù danh sách các tình trạng liên quan béo phì trong bảng không đầy đủ. Bảng được mã màu như sau:
- Màu xanh: có bằng chứng lợi ích.
- Màu xám: chưa đủ bằng chứng nhưng vẫn có thể cân nhắc dùng thuốc.
- Màu vàng: cần thận trọng hoặc theo dõi sát.
- Màu cam: có chống chỉ định đã biết.
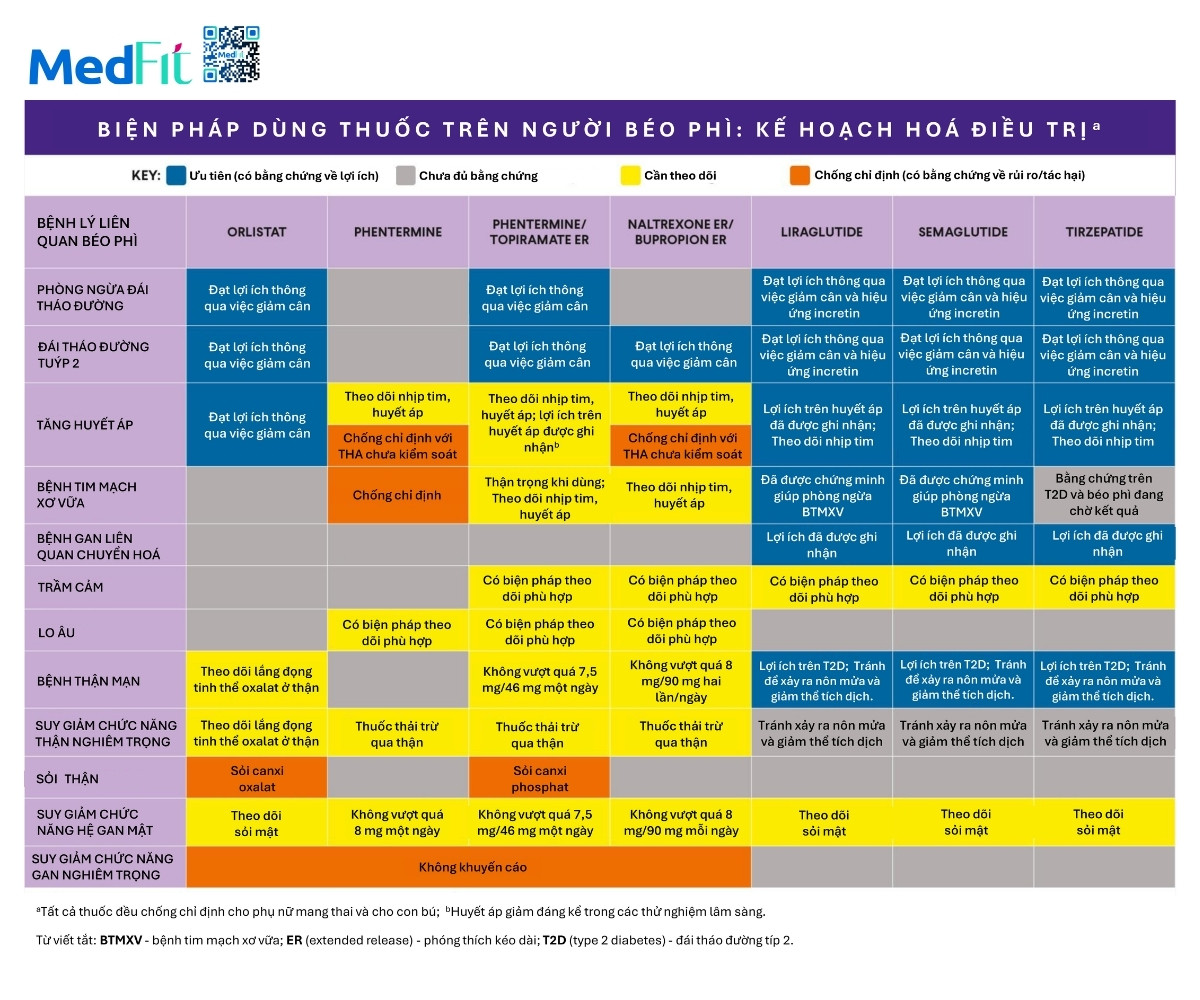
Bác sĩ cần tham khảo thêm thông tin chi tiết trong tờ hướng dẫn kê toa của FDA cho từng thuốc.
Lưu đồ 11 tóm tắt những điểm chính khi kê thuốc điều trị béo phì đã được FDA phê duyệt cho quản lý cân nặng mạn tính gồm tuổi dùng, liều khởi đầu, cách tăng liều, hiệu quả quan sát được, chi phí và các cảnh báo hay chống chỉ định. Tài liệu cũng cung cấp thêm những điểm quan trọng cho từng thuốc tập trung vào kết quả ở quần thể người béo phì. Bác sĩ được khuyến khích đọc kỹ nhãn thuốc do FDA phê duyệt cho từng loại để nắm rõ hơn.
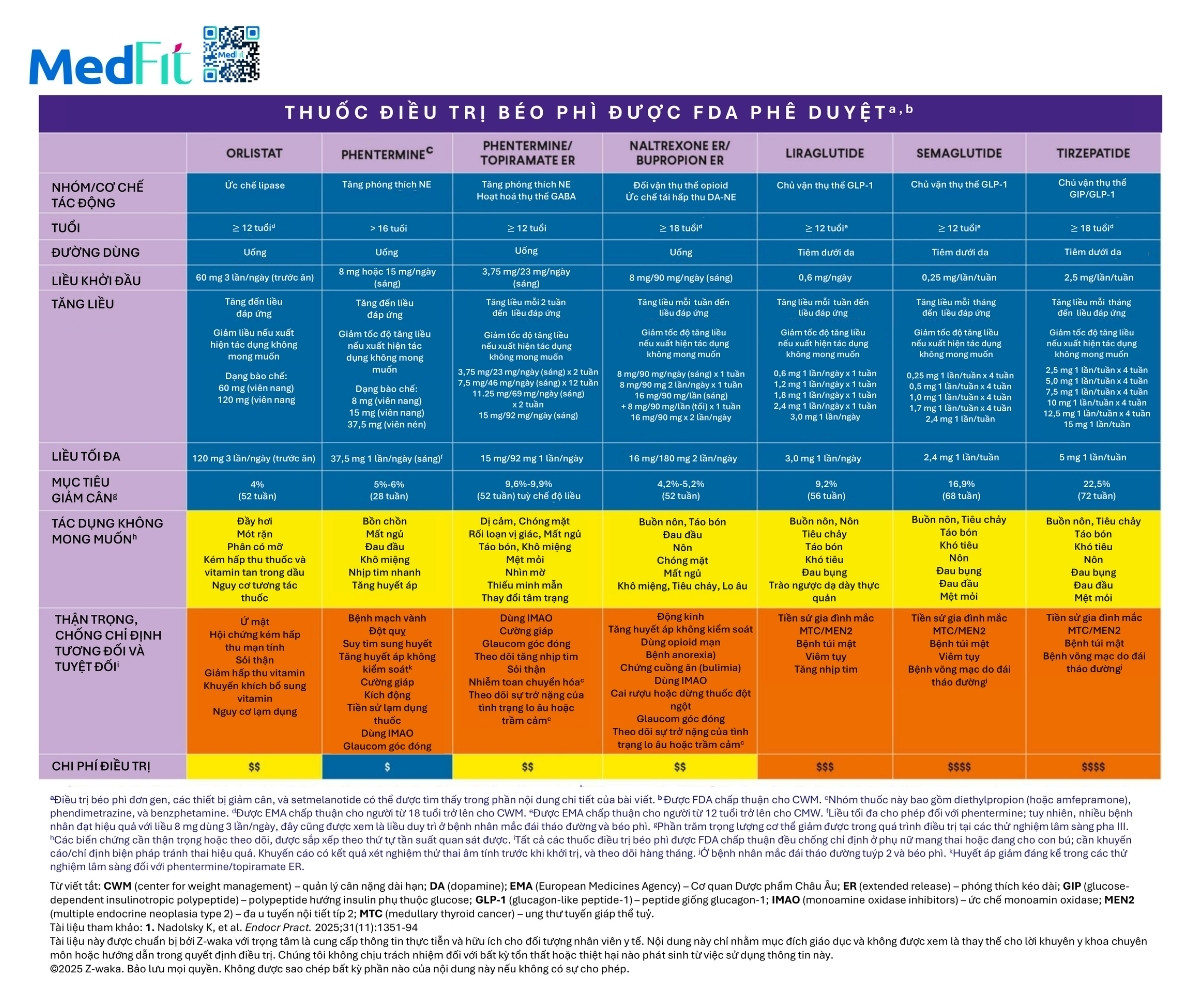
Orlistat
Orlistat được FDA phê duyệt điều trị béo phì mạn tính từ năm 1999. Thuốc giúp giảm cân bằng cách ức chế men lipase tụy và dạ dày, từ đó giảm khoảng 30% hấp thu chất béo. Trong nghiên cứu XENDOS về phòng ngừa đái tháo đường ở người béo phì, sau 4 năm, mức giảm cân trung bình ở nhóm dùng orlistat lớn hơn đáng kể so với nhóm giả dược (5,8 so với 3kg).
Điều trị bằng orlistat cũng giúp giảm rõ rệt tỷ lệ tích lũy mắc đái tháo đường típ 2 sau 4 năm (9% ở nhóm giả dược so với 6,2% ở nhóm orlistat), tương ứng giảm nguy cơ 37,3%. Một lợi ích khác là orlistat giúp giảm LDL cholesterol vượt quá mức mong đợi chỉ nhờ giảm cân.
Hiện có hai liều orlistat được FDA phê duyệt trong điều trị béo phì gồm dạng kê toa 120mg uống 3 lần/ngày trước bữa ăn và dạng không kê toa 60mg uống 3 lần/ngày trước bữa ăn.
Tác dụng phụ của orlistat gồm phân mỡ, són phân, vệt dầu dính, đi tiêu nhiều lần, đau bụng, trung tiện kèm dịch và mót rặn đặc biệt khi ăn nhiều chất béo. Nồng độ vitamin tan trong dầu A, D, E, K trong máu có xu hướng thấp hơn so với giả dược nên khuyến nghị bổ sung vitamin tan trong dầu vào buổi tối hoặc ít nhất 2 giờ sau khi uống orlistat.
Cần theo dõi chức năng gan và thận trong quá trình điều trị. Một số biến cố hiếm nhưng nặng đã được ghi nhận gồm tổn thương gan, sỏi mật, sỏi thận và tổn thương thận. Orlistat không được khuyến cáo cho người có hội chứng kém hấp thu.
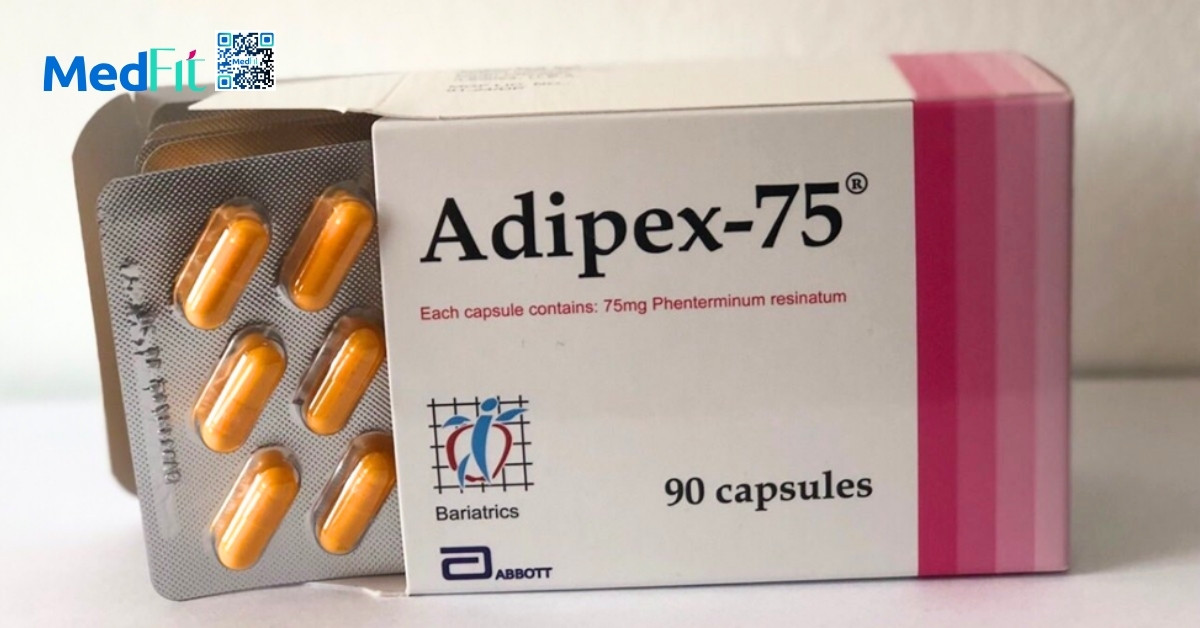
Phentermine và các thuốc giải phóng norepinephrin trung ương khác
Phentermine là thuốc giải phóng norepinephrin trung ương được phê duyệt từ năm 1959 để hỗ trợ giảm cân ngắn hạn trong vài tuần theo nhãn FDA Hoa Kỳ. Vì béo phì là bệnh mạn tính phentermine thường được kê dùng ngoài chỉ định trong thời gian dài hơn 3 tháng và là thuốc điều trị béo phì được kê nhiều nhất tại Hoa Kỳ.
Những lo ngại về an toàn tim mạch dài hạn đang được giải quyết qua thử nghiệm LEAP do Viện Y tế Quốc gia tài trợ nhằm đánh giá hiệu quả và an toàn lâu dài của phentermine. Các nghiên cứu ở người trưởng thành cho thấy phentermine chỉ gây thay đổi huyết áp thoáng qua, còn dữ liệu hồi cứu cho thấy nhìn chung an toàn và hiệu quả dài hạn.
Phentermine có dạng viên hoặc nang. Liều khởi đầu khuyến nghị là 8 hoặc 15mg với liều tối đa 37,5mg uống 1 lần/ngày hoặc 8mg 3 lần/ngày, tổng cộng 24mg. Các nghiên cứu ngắn hạn từ 12-28 tuần ghi nhận mức giảm cân trung bình từ 5,45-7,7% với phentermine. Phần lớn dữ liệu dài hạn đến từ các thử nghiệm dùng kết hợp phentermine và topiramate trong đó thuốc được sử dụng đến 2 năm.
Tác dụng phụ thường gặp của phentermine gồm đau đầu, tăng nhẹ huyết áp và nhịp tim, mất ngủ, khô miệng, táo bón và bồn chồn lo lắng. Phentermine chống chỉ định cho người có bệnh tim mạch như bệnh mạch vành, tăng huyết áp khó kiểm soát, loạn nhịp tim, tiền sử đột quỵ, suy tim, cường giáp, glaucoma và người có tiền sử lạm dụng chất kích thích cùng với phụ nữ mang thai hoặc cho con bú. Các thuốc khác trong nhóm giải phóng norepinephrin được phê duyệt điều trị béo phì gồm diethylpropion, phendimetrazine và benzphetamine.
Phentermine kết hợp topiramate giải phóng kéo dài
Phối hợp phentermine và topiramate dạng giải phóng kéo dài được FDA phê duyệt điều trị quản lý cân nặng mạn tính ở người lớn năm 2012 và cho thanh thiếu niên từ 12 tuổi trở lên năm 2022. Hiệu quả và an toàn đã được đánh giá trong nhiều thử nghiệm ngẫu nhiên có đối chứng. Cơ chế giúp giảm cân của topiramate chưa được hiểu hoàn toàn nhưng được cho là liên quan đến điều hòa giải phóng GABA và ức chế phóng thích glutamat.
Có 4 mức liều uống. Liều khởi đầu 3,75mg phentermine với 23mg topiramate mỗi ngày trong 14 ngày sau đó tăng lên liều duy trì 7,5mg phentermine với 46mg topiramate mỗi ngày. Hai mức liều cao hơn là 11mg với 69mg và 15mg với 92mg dùng trong trường hợp cần kiểm soát cân nặng nhiều hơn. Các thử nghiệm EQUIP CONQUER và SEQUEL ghi nhận nhóm sử dụng phentermine kết hợp topiramate giải phóng kéo dài giảm trung bình 7,8-10,7% cân nặng trong khi nhóm giả dược chỉ giảm 1,2-2,2% khi tính ở cả phân tích người hoàn tất và phân tích theo ý định điều trị.
Hồ sơ tác dụng phụ của phentermine cộng topiramate giống phentermine, kèm thêm tác dụng không mong muốn của topiramate. Các tác dụng phụ thường gặp của topiramate gồm rối loạn vị giác, dị cảm, tác dụng lên nhận thức như buồn ngủ hoặc khó tìm từ và táo bón. Topiramate còn có thể gây hạ kali máu, toan chuyển hóa và sỏi thận vì là chất ức chế men carbonic anhydrase.
Phối hợp phentermine và topiramate giải phóng kéo dài chống chỉ định ở phụ nữ mang thai hoặc cho con bú, người glaucoma và cường giáp chưa điều trị vì topiramate có nguy cơ gây dị tật bẩm sinh. FDA yêu cầu áp dụng chương trình đánh giá và giảm thiểu nguy cơ đối với thuốc này để bảo đảm các nhà thuốc và người có khả năng sinh sản được thông tin rõ về nguy cơ dị tật thai. Cần phòng tránh thai tuyệt đối. Khuyến nghị thử thai âm tính trước khi bắt đầu và kiểm tra hằng tháng. Nếu có thai thuốc phải được ngưng ngay. Người dùng liều cao dễ gặp tác dụng phụ hơn.
Hiện chưa có dữ liệu an toàn tim mạch đầy đủ cho phentermine kết hợp topiramate giải phóng kéo dài, tuy vậy dữ liệu từ các thử nghiệm giai đoạn 3 không cho thấy tín hiệu lo ngại. Tăng nhẹ nhịp tim thường được bù lại bằng giảm huyết áp nên tích số tần số huyết áp vẫn thuận lợi.
Phentermine kết hợp topiramate giải phóng kéo dài đã được chứng minh giúp cải thiện OSA, phòng ngừa tiến triển từ hội chứng chuyển hóa hoặc tiền đái tháo đường sang đái tháo đường típ 2 và ở người mắc đái tháo đường típ 2 giúp giảm cân hạ HbA1c và giảm nhu cầu dùng thuốc hạ đường huyết thông thường.

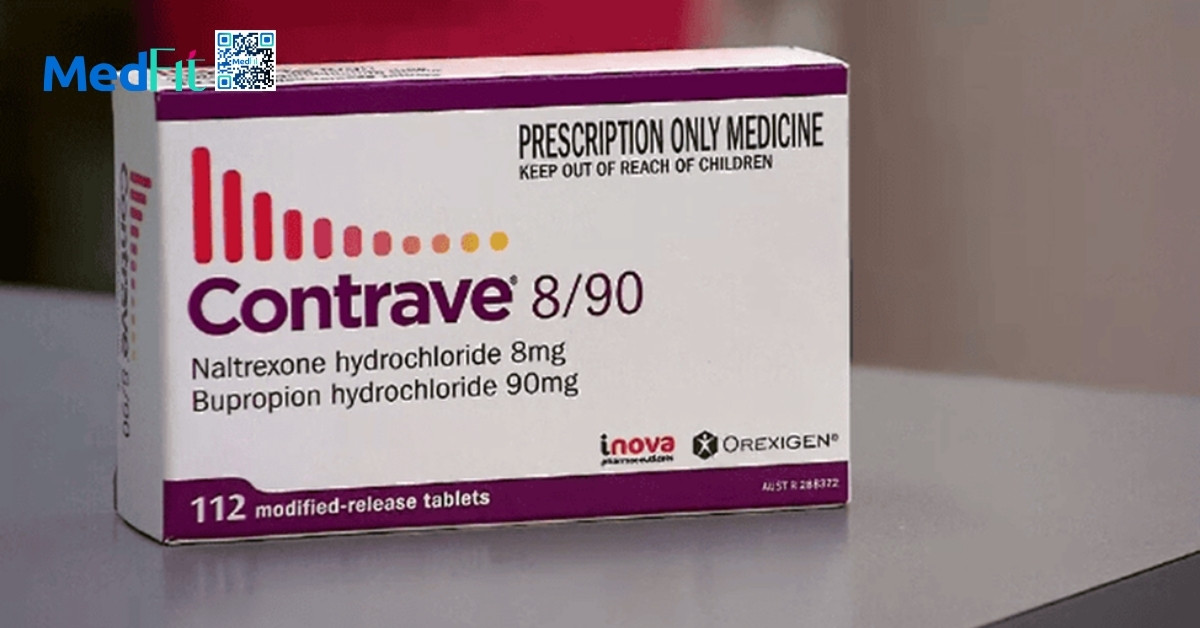
Naltrexone kết hợp bupropion giải phóng kéo dài
Naltrexone kết hợp bupropion dạng giải phóng kéo dài là sự phối hợp giữa naltrexone, thuốc đối kháng opioid và bupropion, thuốc chống trầm cảm ức chế tái thu nhận noradrenalin và dopamin được FDA phê duyệt năm 2014 để điều trị quản lý cân nặng mạn tính ở người trưởng thành. Cơ chế chính xác chưa được hiểu hoàn toàn nhưng các nghiên cứu gợi ý rằng phối hợp này tạo hiệu ứng hiệp lực trong điều hòa lượng thức ăn nạp vào thông qua tác động lên vùng dưới đồi nơi điều hòa cảm giác đói và hệ dopamin trung não viền liên quan cảm giác thưởng.
Mỗi viên naltrexone kết hợp bupropion giải phóng kéo dài chứa 8mg naltrexone và 90mg bupropion. Liều được tăng dần bắt đầu 1 viên/ngày trong 7 ngày đầu sau đó tăng thêm 1 viên/tuần cho đến liều tối đa 2 viên x 2 hai lần/ngày tương đương 32mg naltrexone và 360mg bupropion. Cần thận trọng khi dùng cho người trên 65 tuổi vì có thể nhạy hơn với tác dụng phụ trên hệ thần kinh trung ương. Chưa có dữ liệu an toàn và hiệu quả ở người dưới 18 tuổi nên không khuyến cáo sử dụng.
Trong 4 thử nghiệm giai đoạn 3 kéo dài 56 tuần điều trị bằng naltrexone kết hợp bupropion liều 32mg với 360 mg mang lại mức giảm cân lâm sàng có ý nghĩa dao động từ 5,9-11,5% so với giả dược ở nhóm hoàn tất. Ba thử nghiệm đầu tập trung vào người béo phì đơn thuần hoặc béo phì kèm tăng huyết áp và rối loạn lipid đã kiểm soát. Những người đạt giảm tối thiểu 5% cân nặng trong 3 tháng đầu ở liều tối đa ghi nhận mức giảm trung bình gần 12%.
Naltrexone kết hợp bupropion giải phóng kéo dài không nên dùng cùng bữa ăn nhiều chất béo vì có thể làm tăng đáng kể nồng độ thuốc trong máu. Cần chỉnh liều cho người suy thận hoặc suy gan. Liều tối đa là 1 viên x 2 lần/ngày ở người suy thận trung bình đến nặng hoặc suy gan trung bình. Không khuyến cáo dùng cho người bệnh thận giai đoạn cuối hoặc suy gan nặng.
Tác dụng phụ thường gặp gồm buồn nôn, đau đầu, táo bón, chóng mặt, nôn và khô miệng với tần suất khoảng 4-32%. Có ghi nhận tăng nhẹ huyết áp và nhịp tim nên cần theo dõi hai chỉ số này lúc khởi trị và định kỳ sau đó.
Một thử nghiệm kết cục tim mạch đã được khởi động nhưng bị dừng do dữ liệu bị lộ ra công chúng trước thời hạn nên hiện chưa có kết luận đầy đủ về an toàn tim mạch. Cần thận trọng khi dùng chung với thuốc chẹn beta vì naltrexone kết hợp bupropion có thể làm tăng nồng độ nhóm thuốc này. Nên bắt đầu với liều thấp và theo dõi sát nhịp tim.
Chống chỉ định gồm tăng huyết áp không kiểm soát, tiền sử co giật vì bupropion có thể làm giảm ngưỡng co giật, chán ăn tâm thần hoặc bulimia, ngưng đột ngột rượu, benzodiazepin, barbiturat hoặc thuốc chống động kinh, đang dùng thuốc chứa bupropion khác, sử dụng opioid mạn tính, dùng đồng thời hoặc trong vòng 14 ngày sau thuốc ức chế monoamin oxydase, dị ứng với thành phần thuốc và phụ nữ mang thai.
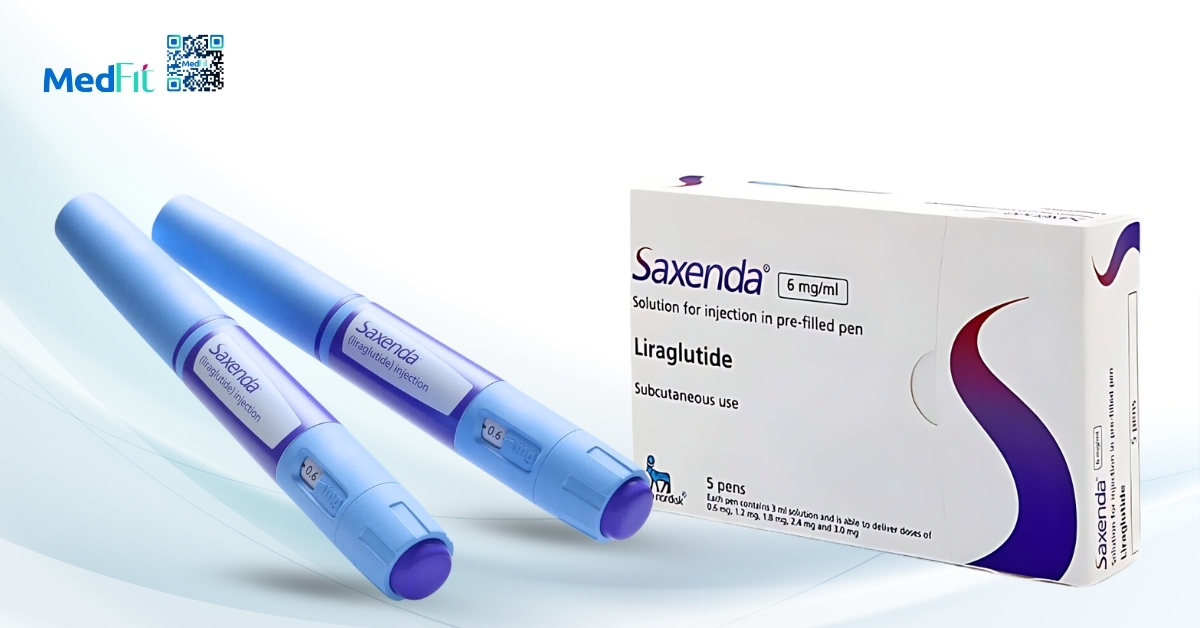
Liraglutide
Liraglutide là thuốc đồng vận thụ thể GLP-1 (GLP-1RA) tiêm dưới da hằng ngày. Thuốc được FDA phê duyệt điều trị đái tháo đường típ 2 từ năm 2010 với liều 1,8mg/ngày. Đến năm 2014, liraglutide trở thành GLP-1RA đầu tiên được FDA chấp thuận cho điều trị kiểm soát cân nặng mạn tính ở người lớn béo phì và năm 2020 mở rộng cho thanh thiếu niên với liều 3mg/ngày.
Ngoài tác dụng incretin đã được mô tả rõ, GLP-1 nội sinh còn tham gia điều hòa cân nặng thông qua tác động trung ương tại nhiều vùng não, đặc biệt vùng dưới đồi bằng cách hoạt hóa trực tiếp các neuron POMC và CART, đồng thời ức chế gián tiếp các neuron NPY và AgRP, bên cạnh đó còn có tác động ở thân não.
Liraglutide có thời gian bán thải khoảng 13 giờ nên dùng 1 lần/ngày. Liều được tăng dần mỗi tuần theo khả năng dung nạp, khởi đầu 0,6mg/ngày. Liraglutide được FDA phê duyệt điều trị béo phì mạn tính cho người từ 12 tuổi trở lên với liều 3mg/ngày.
Hiệu quả và độ an toàn ở người lớn được đánh giá trong nghiên cứu SCALE Obesity and Prediabetes. Sau 56 tuần, nhóm liraglutide 3mg giảm trung bình 8% cân nặng so với 2,6% ở nhóm giả dược. Có 63,2% người dùng liraglutide giảm được ít nhất 5% cân nặng so với 20,71% ở nhóm giả dược. Liraglutide 3mg cũng giúp ngăn tiến triển từ tiền đái tháo đường sang đái tháo đường típ 2.
Ở người béo phì kèm đái tháo đường típ 2, nghiên cứu SCALE Diabetes ghi nhận sau 56 tuần nhóm liraglutide 3mg giảm trung bình 5,8% cân nặng so với 1,5% ở nhóm giả dược. Có 51,8% người sử dụng liraglutide đạt giảm ít nhất 5% cân nặng so với 24% ở nhóm giả dược.
Liraglutide đồng thời cải thiện rõ rệt HbA1c với mức giảm trung bình 1,3% so với 0,3% ở nhóm giả dược cải thiện đường huyết lúc đói và sau ăn và giảm glucagon lúc đói. Mức giảm cân từ 4% trở lên tại tuần 16 được xem là yếu tố dự báo tốt cho giảm cân ở tuần 56 ở cả nhóm có và không có đái tháo đường.
Thử nghiệm LEADER cho thấy liraglutide liều 1,8mg/ngày giúp giảm rõ rệt các biến cố tim mạch chính gồm tử vong do tim mạch, nhồi máu cơ tim không tử vong và đột quỵ không tử vong ở người đái tháo đường típ 2 có nguy cơ tim mạch cao. Chưa có thử nghiệm kết cục tim mạch ở người béo phì không mắc đái tháo đường dùng liraglutide.
Các tác dụng phụ chính và cách giảm nhẹ của liraglutide được trình bày chung trong phần nói về nhóm thuốc dựa trên hormone kích thích bởi chất dinh dưỡng, bao gồm các GLP-1RA được FDA phê duyệt để điều trị béo phì như liraglutide, semaglutide và tirzepatide.
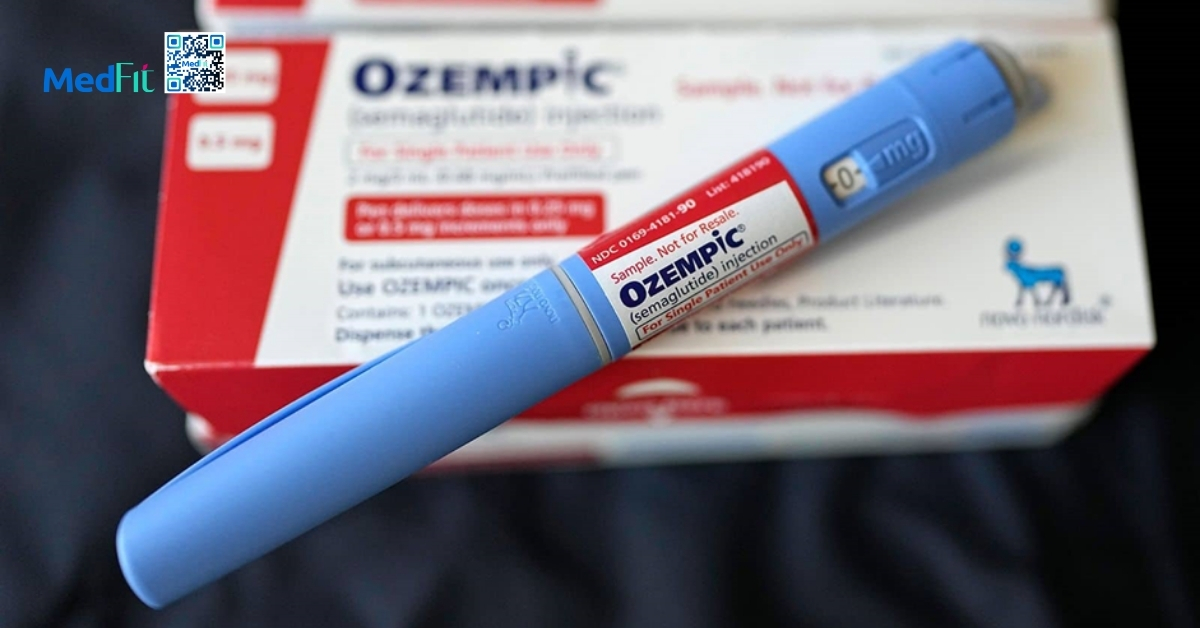
Semaglutide
Semaglutide là thuốc đồng vận thụ thể GLP-1 thế hệ 2 có dạng tiêm dưới da mỗi tuần và dạng uống hằng ngày. Dạng tiêm có thời gian bán thải khoảng 183 giờ. Liều 2,4mg/tuần được FDA phê duyệt điều trị béo phì ở người lớn năm 2021 và cho thanh thiếu niên từ 12 tuổi trở lên năm 2022. Thuốc được phê duyệt điều trị đái tháo đường típ 2 từ năm 2017 với các liều 1-2mg/tuần và gần đây liều 2,4mg/tuần còn được phê duyệt để giảm nguy cơ tim mạch thứ phát.
Trong điều trị béo phì, semaglutide dạng tiêm được tăng liều từ 0,25mg/tuần rồi tăng dần mỗi tháng theo dung nạp đến tối đa 2,4mg/tuần. Dạng uống được FDA phê duyệt điều trị đái tháo đường típ 2 với liều 14mg/ngày và trong các thử nghiệm pha 3 ở người béo phì cho thấy hiệu quả với liều 25-50mg/ngày.
Thử nghiệm STEP 1 cho thấy, semaglutide 2,4mg giúp giảm cân trung bình 16,9% sau 68 tuần điều trị. Thử nghiệm STEP 5 ghi nhận mức giảm 16,7% vẫn duy trì sau năm điều trị thứ hai. Thử nghiệm OASIS một đánh giá semaglutide dạng uống liều 50mg/ngày trong 68 tuần ghi nhận giảm trung bình 17,1%. Một số thử nghiệm pha 3 khác đang đánh giá các liều tiêm cao hơn như 7,2mg/tuần ở người béo phì kèm đái tháo đường típ 2.
Trong thử nghiệm SUSTAIN FORTE semaglutide tiêm 2mg/tuần giúp giảm HbA1c 2,2% so với 1,9% ở nhóm 1mg/tuần trên bệnh nhân đái tháo đường típ 2.
Các dữ liệu trước đây cho thấy, semaglutide làm giảm biến cố tim mạch chính ở người béo phì kèm đái tháo đường típ 2 có bệnh mạch vành hoặc nguy cơ tim mạch cao. Thử nghiệm SELECT là thử nghiệm kết cục tim mạch đầu tiên đánh giá dự phòng thứ phát ở người có bệnh tim mạch xơ vữa đã xác định kèm béo phì nhưng không mắc đái tháo đường.
Điều trị bằng semaglutide 2,4mg/tuần giúp giảm 20% nguy cơ 3 biến cố tim mạch MACE gồm nhồi máu cơ tim không tử vong, đột quỵ không tử vong và tử vong do tim mạch sau trung bình 34 tháng điều trị và 40 tháng theo dõi từ đó được FDA phê duyệt cho mục đích giảm nguy cơ tim mạch thứ phát.
Semaglutide 2,4mg cũng được chứng minh giúp ngăn tiến triển từ tiền đái tháo đường sang đái tháo đường típ 2 làm chậm suy giảm chức năng thận ở bệnh nhân đái tháo đường típ 2 ở liều điều trị đái tháo đường cải thiện thoái hóa khớp gối và HFpEF và cải thiện mô bệnh học cùng xơ hóa trong MASH. Các tác dụng phụ và chiến lược giảm nhẹ được nêu trong phần trình bày chung về nhóm GLP-1RA sử dụng điều trị béo phì.
Tirzepatide
Tirzepatide là thuốc điều trị béo phì thế hệ 2 và là thuốc đầu tiên trong nhóm đồng vận kép GIP và GLP-1 được FDA phê duyệt. Đây là phân tử đơn được thiết kế từ trình tự GIP tự nhiên có hoạt tính trên cả thụ thể GIP và GLP-1 nên được xếp vào nhóm chủ vận kép GIP, GLP-1. Tương tự các liệu pháp dựa trên hormone kích thích sau ăn khác, tirzepatide tác động trung ương lên điều hòa cảm giác đói và kiểm soát cân nặng.
Tirzepatide được bào chế dạng tiêm dưới da mỗi tuần với thời gian bán thải khoảng 116,7 giờ. Liều được tăng dần mỗi tháng từ liều khởi đầu 2,5mg/tuần đến tối đa 15mg/tuần. FDA phê duyệt các liều 5-10mg và 15mg/tuần để điều trị béo phì từ năm 2023 và điều trị đái tháo đường típ 2 từ năm 2022.
Các thử nghiệm SURMOUNT đánh giá hiệu quả và tính an toàn của tirzepatide ở người béo phì. Trong SURMOUNT-1 liều 15mg giúp giảm cân trung bình 22,5% sau 72 tuần và gần 40% người bệnh đạt giảm ít nhất 25% cân nặng. SURMOUNT-3 và SURMOUNT-4 cho thấy khi kết hợp với can thiệp lối sống chuyên sâu hoặc kéo dài điều trị đến 88 tuần mức giảm cân có thể đạt 26,6% và 26%.
Hiệu quả giảm cân thường thấp hơn ở người đái tháo đường típ 2. Trong SURMOUNT-2, tirzepatide giúp giảm trung bình 12,8% và 14,7% cân nặng tương ứng với liều 10mg và 15mg đồng thời giảm HbA1c 2,2% gần một nửa số người đạt HbA1c dưới 5,7% và gần như không gặp hạ đường huyết mức độ 2 hoặc 3.
Các thử nghiệm SURPASS đánh giá hiệu quả ở bệnh nhân đái tháo đường típ 2 ghi nhận giảm HbA1c từ 1,9-2% và hơn 87% người đạt mục tiêu HbA1c dưới 7%.
Trong phân tích hậu kiểm đã định trước, tirzepatide không làm tăng nguy cơ biến cố tim mạch chính so với nhóm đối chứng. Thử nghiệm kết cục tim mạch SURPASS CVOT ở người đái tháo đường típ 2 đang tiến hành và thử nghiệm SURMOUNT MMO đang đánh giá dự phòng nguyên phát và thứ phát biến cố tim mạch ở người béo phì không mắc đái tháo đường.
Tirzepatide được chứng minh giúp ngăn tiến triển từ tiền đái tháo đường sang đái tháo đường típ 2 cải thiện OSA, HFpEF và cải thiện mô bệnh học cùng xơ hóa trong MASH. Tháng 12/2024, FDA phê duyệt tirzepatide là thuốc kê toa đầu tiên điều trị OSA mức độ vừa đến nặng ở người lớn béo phì.
Các tác dụng phụ chính của tirzepatide và chiến lược giảm nhẹ được trình bày chung trong phần nói về nhóm GLP-1RA điều trị béo phì gồm liraglutide, semaglutide và tirzepatide.
Giảm nhẹ tác dụng phụ của các liệu pháp dựa trên hormone kích thích sau ăn
Tác dụng phụ thường gặp nhất của nhóm thuốc dựa trên GLP-1 như liraglutide, semaglutide và tirzepatide là rối loạn tiêu hóa, xuất hiện nhiều nhất trong giai đoạn tăng liều. Với người chưa từng dùng nhóm này nên khởi đầu ở liều thấp nhất để giảm nguy cơ tác dụng phụ rõ rệt, đồng thời tăng liều từ từ sẽ giúp cơ thể thích nghi tốt hơn.
Người dùng được khuyến khích theo dõi những loại thức ăn làm nặng thêm triệu chứng, ví dụ thức ăn nhiều dầu mỡ, tránh ăn vượt quá cảm giác no và có thể chia nhỏ bữa ăn, ăn nhiều lần với khẩu phần nhỏ hơn. Nếu tạm ngưng điều trị trong một thời gian, khi dùng lại cần quay về liều thấp và tăng dần để cơ thể có thời gian thích nghi.
Nhóm GLP-1RA cũng gây tăng nhẹ nhịp tim. Người có nôn ói hoặc tiêu chảy cần được theo dõi nguy cơ mất nước và suy thận. Điều trị có thể làm tăng lipase và amylase huyết thanh dù không có viêm tụy. Việc giảm cân từ bất kỳ phương thức nào đều làm tăng nguy cơ bệnh túi mật, dùng GLP-1RA có vẻ làm nguy cơ này tăng thêm.
FDA khuyến nghị tiếp tục theo dõi sát các thay đổi về tâm trạng, biểu hiện mới hoặc nặng lên của trầm cảm hay ý tưởng tự sát trong quá trình điều trị bằng GLP-1RA dù cả FDA và Cơ quan Dược châu Âu đều cho rằng bằng chứng hiện tại chưa đủ để khẳng định mối liên hệ nhân quả.
Setmelanotide
Setmelanotide là thuốc đồng vận thụ thể melanocortin 4 (MC4R) dùng tiêm dưới da hằng ngày để điều trị một số rối loạn di truyền hiếm gây béo phì. Thuốc được FDA cấp quy chế thuốc đột phá năm 2020 cho chỉ định quản lý cân nặng mạn tính ở người từ 6 tuổi trở lên có béo phì do thiếu POMC, thiếu men proprotein convertase 1 hoặc thiếu thụ thể leptin. Tháng 6/2022 thuốc tiếp tục được phê duyệt điều trị hội chứng Bardet Biedl và cho thấy hiệu quả ở người béo phì do tổn thương vùng dưới đồi.
Setmelanotide tác động lên MC4R, thụ thể giữ vai trò trung tâm trong kiểm soát cảm giác đói và cân bằng năng lượng. Người có đột biến gen ảnh hưởng đường truyền tín hiệu MC4R thường khởi phát béo phì rất sớm trước 5 tuổi, kèm ăn nhiều không kiểm soát và tiền sử gia đình béo phì rõ rệt.
Vì các đột biến này rất hiếm nên phê duyệt ban đầu dựa trên các nghiên cứu gồm 21 người. Trong 10 người thiếu POMC hoặc thiếu proprotein convertase 1 có 8 người đạt tiêu chí chính là giảm ít nhất 10% cân nặng sau 1 năm, mức giảm trung bình đạt 25,6%. Trong 11 người thiếu thụ thể leptin đáp ứng biến thiên hơn chỉ 5 người đạt giảm ít nhất 10% cân nặng sau 1 năm.
Trong nghiên cứu trên người mắc Bardet Biedl syndrome, 16 người từ 12 tuổi trở lên được điều trị setmelanotide và 32,3% trong số này giảm ít nhất 10% cân nặng sau 52 tuần. Các nghiên cứu về chất lượng cuộc sống ở 20 người mắc hội chứng Bardet Biedl cũng ghi nhận cải thiện rõ rệt trên nhiều thang điểm sau 1 năm điều trị. Người béo phì do tổn thương vùng dưới đồi cũng cho thấy hưởng lợi từ setmelanotide.
Tác dụng phụ thường gặp nhất gồm phản ứng tại chỗ tiêm, tăng sắc tố da thường cải thiện sau khi ngưng thuốc, buồn nôn, nôn và tiêu chảy. Các tác dụng phụ khác gồm cương dương tự phát, tăng ham muốn ở nữ, trầm cảm và ý tưởng tự sát.
Hydrogel cellulose và citric acid
Sản phẩm kết hợp cellulose và hydrogel acid citric khác với các thuốc giảm cân khác vì đây không phải là thuốc mà là chất nền không hấp thu trong đường tiêu hóa, chiếm chỗ trong dạ dày nhằm tạo cảm giác no. Sản phẩm được xem là thực phẩm chức năng với chứng nhận FDA cho kiểm soát cân nặng. Trong các nghiên cứu GLOW và GLOW EX, có 59% người dùng đạt giảm ít nhất 5% cân nặng.
Sản phẩm cần tránh ở người có tiền sử bệnh lý tiêu hóa và có thể ảnh hưởng hấp thu các thuốc khác. Plenity đã được nhà sản xuất ngưng cung cấp từ năm 2023 vì lý do tài chính. Một hydrogel khác là epitomee được phê duyệt điều trị người béo phì có BMI từ 25-40 kg/m2, cho mức giảm cân 4,5% sau 12 tuần trong thử nghiệm lâm sàng, đồng thời giảm huyết áp và triglycerid.
Đơn thuốc trực tuyến và các peptide pha chế dựa trên hormone kích thích sau ăn
Kê đơn thuốc điều trị béo phì qua mạng nếu không đi kèm thăm khám lâm sàng bởi nhân viên y tế sẽ không thể đánh giá được các biến chứng liên quan béo phì. Khi thiếu thành phần đánh giá lâm sàng và tầm soát ORCD thì không thể triển khai mô hình điều trị tập trung biến chứng, đồng nghĩa các nguyên tắc chăm sóc chất lượng cho người mắc ABCD trong lưu đồ 1 không thể áp dụng.
Người mắc ABCD cần được theo dõi lâu dài để đánh giá đáp ứng điều trị trên ORCD và duy trì lợi ích sức khỏe. Họ cũng cần được hỗ trợ đảm bảo dinh dưỡng đầy đủ, giảm nhẹ tác dụng phụ, tránh giảm cân thái quá hoặc suy dinh dưỡng đặc biệt khi dùng thuốc thế hệ 2 và xây dựng chiến lược điều trị duy trì an toàn dài hạn có thể khác với phác đồ trong giai đoạn giảm cân tích cực.
Telemedicine và các giải pháp chăm sóc từ xa có thể được ứng dụng trong điều trị ABCD nhưng dù tái khám trực tiếp hay trực tuyến, sự tham gia của đội ngũ y tế được đào tạo vẫn là điều bắt buộc để đạt các mục tiêu trên. Việc kê đơn thuốc điều trị béo phì chỉ qua nền tảng trực tuyến mà không có thăm khám ban đầu và theo dõi bởi nhân viên y tế được xem là chăm sóc dưới chuẩn và có thể đặt người bệnh vào nguy cơ.
Hiện nay, nhiều chế phẩm pha chế thay thế semaglutide và tirzepatide được FDA phê duyệt đang được bán qua các nhà thuốc trực tuyến. AACE khuyến cáo không sử dụng các sản phẩm này. Nhu cầu dùng thuốc pha chế tăng lên do hiệu quả vượt trội của semaglutide và tirzepatide trong khi chi phí cao, bảo hiểm chi trả hạn chế và nguồn cung thuốc gốc thiếu hụt.
Cả tirzepatide và semaglutide đều từng rơi vào tình trạng thiếu hàng do mất cân bằng cung cầu. Theo quy định, các cơ sở pha chế được phép bào chế thuốc tương ứng khi thuốc gốc nằm trong danh mục thiếu hụt của FDA và phải đáp ứng một số điều kiện pháp lý.
Tuy vậy, các thuốc pha chế không được FDA phê duyệt nên không có bước thẩm định trước về độ an toàn, hiệu quả và chất lượng trước khi lưu hành, từ đó tiềm ẩn rủi ro cao hơn so với thuốc gốc. Phân tích một số mẫu thuốc pha chế cho thấy tình trạng ghi sai hàm lượng, lẫn tạp chất, peptide phân tử lượng cao khác, kim loại nặng, dung môi tồn dư và các neo peptide do quy trình tổng hợp hóa học thay vì công nghệ ADN tái tổ hợp, tất cả đều có khả năng gây đáp ứng miễn dịch bất lợi.
FDA đã cảnh báo về nguy cơ quá liều dẫn đến nhập viện ở người dùng semaglutide và tirzepatide pha chế. Các công ty dược liên quan đã đề nghị FDA đưa tirzepatide và semaglutide vào danh sách “gặp khó khăn rõ rệt trong pha chế bào chế” và đề xuất này đã được chấp thuận gần đây. Những thuốc hoặc nhóm thuốc được xếp vào diện “gặp khó khăn rõ rệt trong pha chế bào chế” theo các điều khoản 503A hoặc 503B của Đạo luật Thực phẩm Dược phẩm và Mỹ phẩm Liên bang, việc pha chế thuốc đó sẽ bị cấm.

* Voucher chỉ áp dụng cho khách hàng thăm khám lần đầu tiên tại Phòng khám MedFit
Kết luận
Béo phì là bệnh lý mạn tính, không đồng nhất, thuộc nhóm rối loạn nội tiết thần kinh, có tính tiến triển và dễ tái phát, chịu ảnh hưởng bởi môi trường cùng các yếu tố nhạy cảm di truyền, dẫn đến tình trạng mô mỡ dư thừa hoặc phân bố bất thường làm suy giảm sức khỏe tổng thể.
Hướng dẫn này hỗ trợ Bác sĩ trong quá trình ra quyết định cùng người bệnh khi điều trị y khoa cho bệnh lý mạn tính do tăng mô mỡ (adiposity based chronic disease – ABCD) theo hướng tập trung vào biến chứng, đồng thời đưa ra định hướng hỗ trợ cho các can thiệp lối sống và hành vi được cá nhân hóa.
Đánh giá nhân trắc học kết hợp với đánh giá lâm sàng là nền tảng để chẩn đoán và phân tầng mức độ bệnh, từ đó quyết định cường độ điều trị và thiết lập mục tiêu điều trị phù hợp cho từng cá nhân. Việc đánh giá cần có khai thác bệnh sử tổng quát và bệnh sử liên quan béo phì, khai thác triệu chứng theo cơ quan, khám lâm sàng và chỉ định các xét nghiệm cận lâm sàng cần thiết được thực hiện bởi nhân viên y tế được đào tạo.
Bên cạnh đó, xây dựng kế hoạch chăm sóc cá thể hóa đòi hỏi sự tham gia chủ động của người bệnh trong quá trình ra quyết định và phải cân nhắc yếu tố định kiến, kỳ thị liên quan cân nặng, các rối loạn tâm lý kèm theo và những yếu tố xã hội ảnh hưởng đến sức khỏe.
Mục tiêu lâm sàng không chỉ dừng ở giảm và duy trì cân nặng mà hướng đến trọng tâm là cải thiện các biến chứng liên quan tăng mô mỡ (obesity related complications and diseases – ORCD), cải thiện kết cục sức khỏe và nâng cao chất lượng cuộc sống phù hợp với cách tiếp cận điều trị tập trung vào biến chứng.
Can thiệp lối sống vẫn luôn là trụ cột quan trọng trong tối ưu hóa sức khỏe cho người mắc ABCD. Điều này bao gồm tư vấn dinh dưỡng y học cá thể hóa, kê đơn hoạt động thể lực và các can thiệp hành vi giúp xây dựng thói quen ăn uống lành mạnh, duy trì vận động trong sinh hoạt hằng ngày. Một điểm cốt lõi là người bệnh ABCD cần duy trì các thay đổi về lối sống và hành vi song song với việc khởi trị và tiếp tục sử dụng thuốc điều trị béo phì để tối ưu hóa sức khỏe tổng thể.
Các thuốc điều trị có cơ chế tác động, tác dụng phụ và hiệu quả lâm sàng khác nhau. Việc ra quyết định dựa trên thảo luận chung giữa Bác sĩ và người bệnh giúp cá thể hóa điều trị, lựa chọn loại thuốc phù hợp nhất với đặc điểm bệnh lý, cải thiện chất lượng cuộc sống và hỗ trợ điều trị hoặc dự phòng các biến chứng liên quan tăng mô mỡ. Lần đầu tiên, phác đồ này thiết lập hệ thống phân tầng ưu tiên thuốc trong mô hình điều trị tập trung vào biến chứng dựa trên bằng chứng về khả năng cải thiện từng nhóm ORCD cụ thể.
Quan trọng hơn, tương tự mọi bệnh mạn tính phức tạp khác, việc chăm sóc suốt đời là rất cần thiết. Các biện pháp điều trị béo phì cần được điều chỉnh linh hoạt theo thời gian phù hợp với nhu cầu từng người, với mục tiêu cuối cùng là tối ưu hóa sức khỏe tổng thể trong suốt cuộc đời.
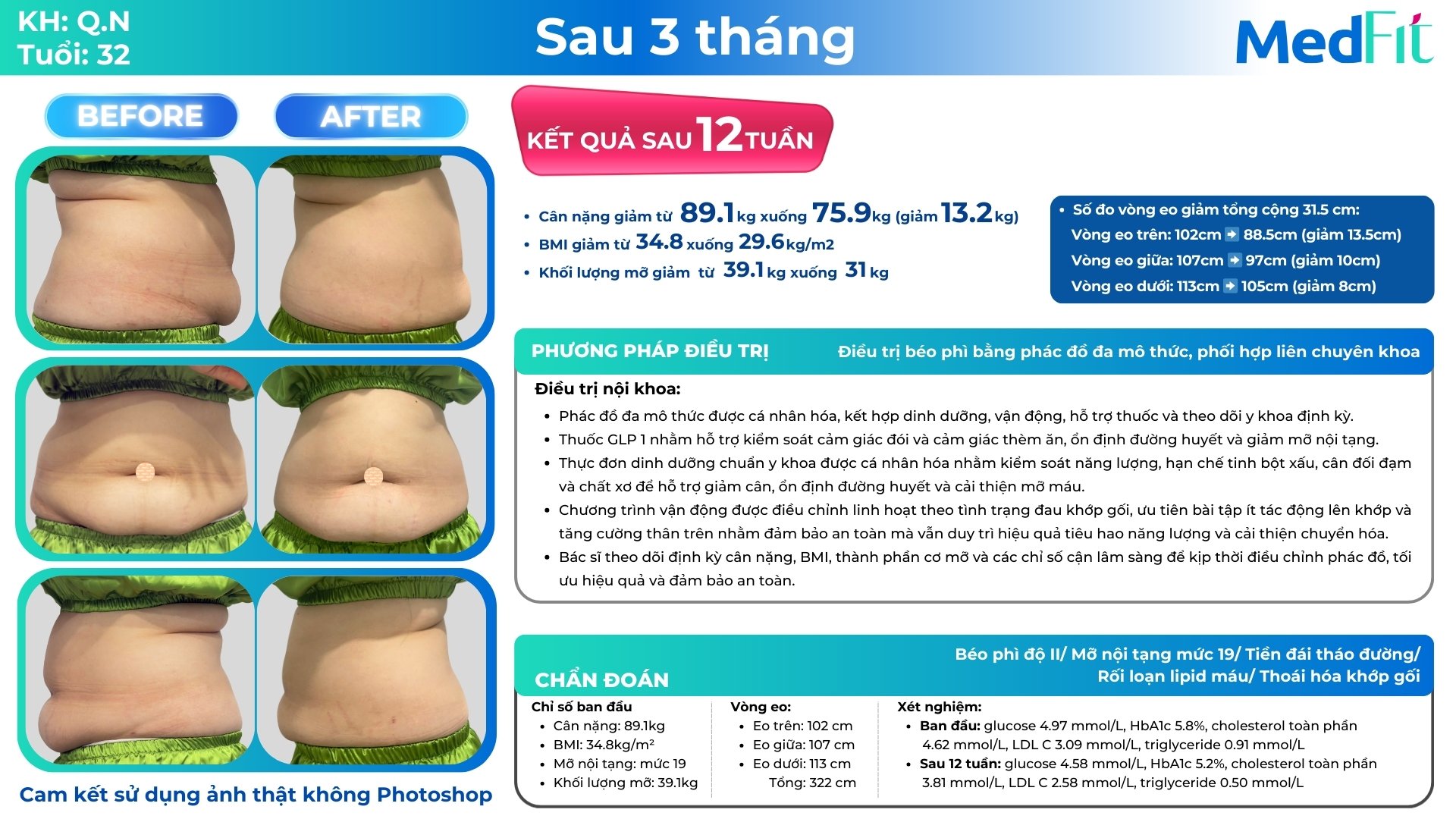
Tại MedFit, kiểm soát béo phì được tiếp cận theo hướng y khoa cá nhân hoá, tập trung vào cải thiện chuyển hoá nền tảng và bảo tồn chức năng sinh học thay vì chỉ giảm cân ngắn hạn. Thông qua thăm khám, đánh giá toàn diện tình trạng mỡ nội tạng, khối cơ và nguy cơ chuyển hoá, Bác sĩ tại MedFit xây dựng phác đồ phù hợp cho từng trường hợp, hướng đến mục tiêu giảm béo an toàn, bền vững và hỗ trợ làm chậm lão hoá.
Nếu đang quan tâm đến việc kiểm soát cân nặng như một chiến lược chăm sóc sức khoẻ dài hạn, MedFit là nơi có thể đồng hành trên hành trình đó một cách bài bản và khoa học.


Tài liệu tham khảo
- Nadolsky K, Garvey WT, Agarwal M, Bonnecaze A, Burguera B, Chaplin MD, Griebeler ML, Harris SR, Schellinger JN, Simonetti J, Srinath R, Yumuk V. American Association of Clinical Endocrinology Consensus Statement: Algorithm for the Evaluation and Treatment of Adults with Obesity/Adiposity-Based Chronic Disease – 2025 Update. Endocr Pract. 2025 Nov;31(11):1351–1394. doi:10.1016/j.eprac.2025.07.017













