Béo phì không chỉ làm thay đổi vóc dáng mà còn kéo theo hàng loạt nguy cơ sức khỏe nghiêm trọng. Nhiều nghiên cứu cho thấy người thừa cân có nguy cơ cao mắc các bệnh lý mạn tính như tăng huyết áp, đái tháo đường, rối loạn mỡ máu và đặc biệt là bệnh thận mạn. Vậy béo phì có gây suy thận không, cơ chế nào đứng sau mối liên hệ này và làm sao để phòng ngừa hiệu quả? Hãy cùng MedFit tìm hiểu chi tiết trong bài viết dưới đây.
Béo phì và tác động lên sức khỏe toàn thân
Các nhà khoa học xem béo phì như một bệnh lý mạn tính, bởi tình trạng này có thể kích hoạt hàng loạt biến đổi chuyển hóa và gia tăng nguy cơ nhiều bệnh nguy hiểm. Béo phì thường chẩn đoán dựa vào chỉ số khối cơ thể (BMI), được tính bằng công thức BMI = cân nặng (kg) chia cho bình phương chiều cao (m²). Theo chuẩn châu Á, thừa cân được xác định khi BMI ≥ 23kg/m² và béo phì khi BMI ≥ 25kg/m².

Bên cạnh BMI, nhiều chỉ số khác cũng được sử dụng để đánh giá tình trạng tích lũy mỡ nội tạng, vốn mang nguy cơ cao đối với rối loạn chuyển hóa và bệnh tim mạch. Vòng eo từ 90cm trở lên ở nam và 80cm trở lên ở nữ được xem là ngưỡng nguy cơ.

Tỷ lệ vòng eo trên hông (waist-to-hip ratio, WHR) vượt quá 0,9 ở nam hoặc 0,85 ở nữ cũng là dấu hiệu cảnh báo. Ngoài ra, tỷ lệ vòng eo trên chiều cao (waist-to-height ratio) từ 0,5 trở lên được xem là ngưỡng nguy cơ rõ rệt. Việc kết hợp các chỉ số này cùng với BMI giúp việc đánh giá mức độ nguy cơ liên quan đến béo phì chính xác hơn thay vì chỉ dựa vào một chỉ số đơn lẻ.
Béo phì đang trở thành một vấn đề sức khỏe cộng đồng nghiêm trọng trên phạm vi toàn cầu. Năm 2022, đã có hơn 1 tỷ người bị béo phì, chiếm khoảng 12,5% dân số thế giới. Các dự báo cho thấy đến năm 2035, hơn một nửa dân số toàn cầu có thể rơi vào tình trạng này, làm gia tăng đáng kể gánh nặng bệnh tật và chi phí điều trị.
Tại Việt Nam, tỷ lệ thừa cân béo phì ở người trưởng thành cũng tăng nhanh trong 30 năm qua, trung bình khoảng 20% và nếu áp dụng chuẩn đánh giá dành cho người châu Á thì con số này có thể lên tới gần 28%.

Thừa cân và béo phì làm gia tăng nguy cơ mắc nhiều vấn đề sức khỏe nghiêm trọng. Các nghiên cứu cho thấy tình trạng này liên quan chặt chẽ đến bệnh thận mạn tính, đái tháo đường típ 2, tăng huyết áp, bệnh tim mạch và đột quỵ. Người béo phì cũng dễ gặp rối loạn giấc ngủ như ngưng thở khi ngủ, gan nhiễm mỡ do tích tụ mỡ trong gan, cũng như thoái hóa khớp gây đau và cứng khớp kéo dài.
Ngoài ra, béo phì còn làm tăng nguy cơ mắc bệnh túi mật, trào ngược dạ dày – thực quản gây ợ nóng và một số loại ung thư, trong đó có ung thư thận. Phụ nữ thừa cân béo phì có thể gặp nhiều biến chứng trong thai kỳ, từ tăng huyết áp thai kỳ cho đến đái tháo đường thai kỳ.
Không chỉ dừng lại ở sức khỏe thể chất, thừa cân béo phì còn ảnh hưởng mạnh đến tinh thần, gây căng thẳng tâm lý và cảm giác tự ti, đặc biệt khi đối diện với sự kỳ thị từ xã hội hoặc thậm chí từ nhân viên y tế.
Cách nhận biết và phân loại bệnh thận mạn
Hiệp hội quốc tế KDIGO về bệnh thận (Kidney Disease Improving Global Outcomes) đã cập nhật hướng dẫn về bệnh thận mạn (Chronic kidney disease – CKD) vào năm 2024, đưa ra định nghĩa và phân loại rõ ràng hơn nhằm hỗ trợ trong chẩn đoán và điều trị.
Bệnh thận mạn được định nghĩa là sự hiện diện các bất thường về cấu trúc hoặc chức năng thận, kéo dài tối thiểu 3 tháng và có ảnh hưởng đến sức khỏe người bệnh. Phân loại CKD theo KDIGO theo tiêu chí CGA gồm:
- C (Cause): nguyên nhân gây bệnh thận
- G (GFR): mức lọc cầu thận ước tính (estimated Glomerular Filtration Rate – eGFR)
- A (Albuminuria): mức độ albumin niệu
Cụ thể:
- G1: GFR ≥ 90mL/phút/1,73m² (bình thường hoặc cao)
- G2: GFR 60-89mL/phút/1,73m² (khi có bằng chứng tổn thương thận)
- G3a: 45-59mL/phút/1,73m²; G3b: 30-44mL/phút/1,73m²
- G4: 15-29mL/phút/1,73m²
- G5: < 15mL/phút/1,73m² (giai đoạn suy thận nặng)
Về albumin niệu:
- A1: < 30mg/g – bình thường hoặc tăng nhẹ
- A2: 30-300mg/g – tăng vừa
- A3: > 300mg/g – tăng nặng
Bảng nguy cơ tiến triển CKD (KDIGO 2024)
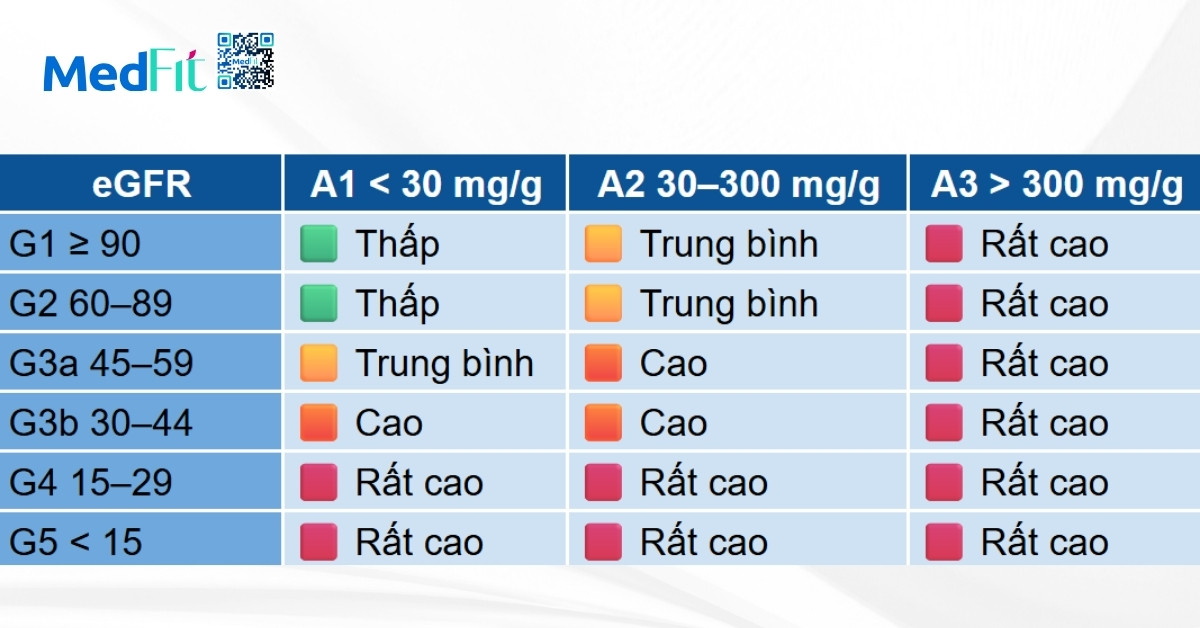
Việc kết hợp eGFR và mức độ albumin niệu giúp phân tầng nguy cơ chính xác hơn, hỗ trợ Bác sĩ tiên lượng tiến triển bệnh, dự phòng biến chứng tim mạch và quyết định thời điểm can thiệp điều trị.

* Voucher chỉ áp dụng cho khách hàng thăm khám lần đầu tiên tại Phòng khám MedFit
Béo phì gây tổn thương thận như thế nào?
Béo phì không chỉ làm tăng nguy cơ gián tiếp thông qua đái tháo đường và tăng huyết áp, mà còn gây ra nhiều thay đổi trực tiếp tại thận. Các cơ chế này phối hợp phức tạp, từ rối loạn huyết động, hoạt động nội tiết của mô mỡ, viêm, stress oxy hóa cho đến thay đổi cấu trúc mô học. Đây chính là nền tảng giải thích vì sao béo phì ngày càng được xem là một yếu tố nguy cơ độc lập của bệnh thận mạn tính.
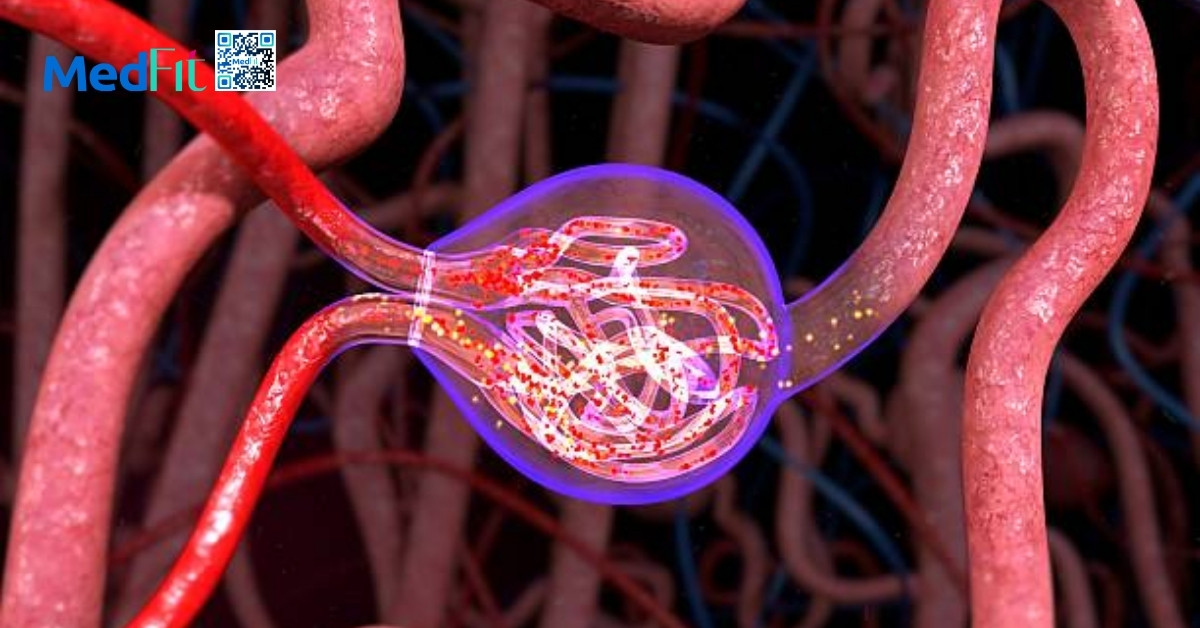
Tăng lọc cầu thận (hyperfiltration)
Ở người béo phì, nhu cầu chuyển hóa tăng khiến thận phải làm việc nhiều hơn. Lưu lượng máu qua thận và áp lực nội cầu thận tăng cao, gây giãn rộng cầu thận và dày màng lọc.
Tình trạng tăng áp lực này kéo dài sẽ phá hủy hàng rào lọc, thúc đẩy protein niệu và tiến triển thành xơ hóa cầu thận. Đây là cơ chế trung tâm hình thành bệnh cầu thận liên quan béo phì (obesity-related glomerulopathy – ORG).
Hoạt hóa hệ renin – angiotensin – aldosterone (RAAS)
Mô mỡ thừa tiết nhiều yếu tố kích thích RAAS, dẫn đến co mạch, giữ muối nước và tăng huyết áp toàn thân. Sự hoạt hóa này làm áp lực cầu thận tăng cao hơn nữa, kết hợp với tăng lọc gây tổn thương cấu trúc thận, thúc đẩy CKD.
Vai trò nội tiết của mô mỡ (adipokine)
Mô mỡ hoạt động như một cơ quan nội tiết, tiết ra nhiều adipokine như leptin, adiponectin và resistin. Ở người béo phì, sự mất cân bằng này làm tăng viêm, rối loạn lipid và ảnh hưởng trực tiếp đến tế bào thận.
Ví dụ, leptin có thể thúc đẩy xơ hóa cầu thận, trong khi giảm adiponectin làm mất cơ chế bảo vệ chống viêm tại thận.
Viêm mạn tính mức độ thấp
Béo phì đi kèm với tình trạng viêm hệ thống do mô mỡ tiết ra nhiều cytokine như TNF-α và IL-6. Viêm kéo dài trong thận dẫn đến thay đổi cấu trúc gian mạch, xơ hóa mô kẽ và suy giảm chức năng lọc máu.
Stress oxy hóa
Tình trạng dư thừa năng lượng và rối loạn chuyển hóa trong béo phì kích thích sản xuất gốc tự do. Stress oxy hóa làm tổn thương màng tế bào, protein và DNA trong thận, đặc biệt ở tế bào biểu mô ống thận và màng lọc cầu thận, thúc đẩy tiến triển CKD.
Đề kháng insulin và rối loạn lipid máu
Đề kháng insulin gây tăng insulin máu mạn tính, làm tăng tái hấp thu natri ở ống thận và góp phần gây tăng huyết áp.
Rối loạn lipid máu thường đi kèm béo phì, cũng dẫn đến lắng đọng lipid bất thường trong thận, gây độc cho tế bào gian mạch và màng đáy cầu thận, từ đó làm nặng thêm tổn thương.
Tích tụ mỡ lạc chỗ trong thận
Ở người béo phì, mỡ có thể tích tụ bất thường tại xoang thận (renal sinus fat) và quanh cầu thận. Tình trạng này làm thay đổi dòng máu thận, tăng áp lực cơ học lên cấu trúc thận và góp phần vào rối loạn chức năng lọc.
Biến đổi mô học đặc hiệu
Các thay đổi mô học điển hình bao gồm giãn lớn cầu thận (glomerulomegaly) và xơ hóa cầu thận từng vùng (focal segmental glomerulosclerosis – FSGS). Đây là dấu hiệu đặc trưng của bệnh cầu thận liên quan béo phì (ORG), một bệnh lý đã tăng gấp 10 lần trong vài thập kỷ qua. Những biến đổi này thường phối hợp với tuổi già hoặc tăng huyết áp, khiến mức độ tổn thương càng nặng.
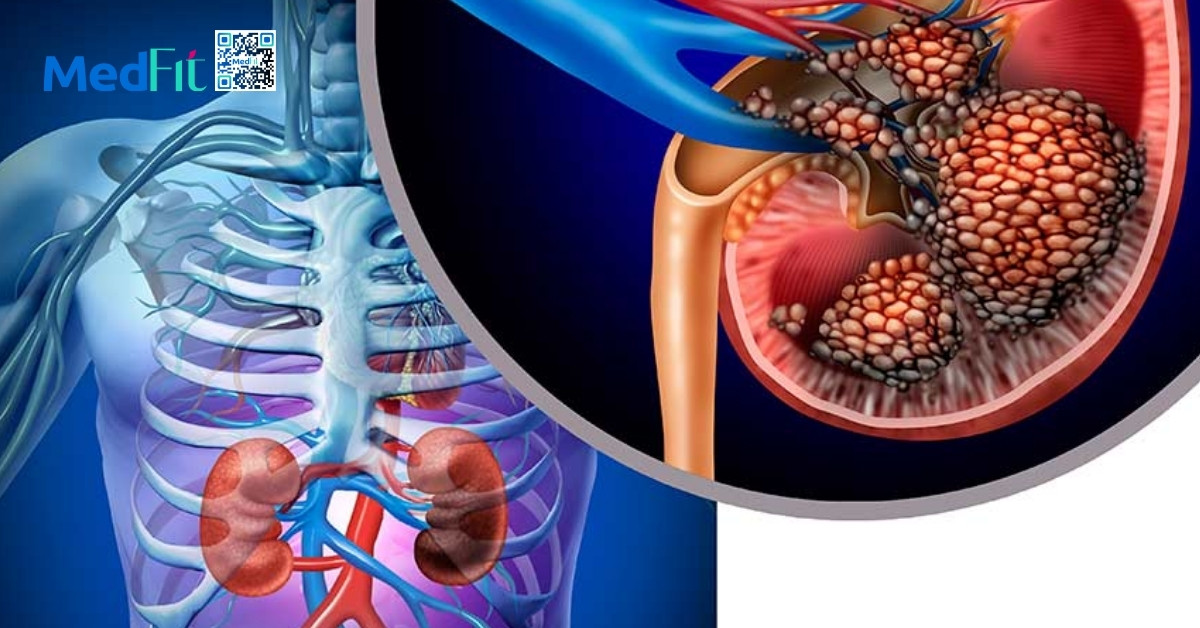
Hình thành sỏi thận (nephrolithiasis)
Béo phì liên quan đến nước tiểu toan tính (pH thấp), tăng bài tiết oxalat, acid uric, natri và phosphate. Đồng thời, chế độ ăn giàu muối và đạm động vật phổ biến ở người béo phì càng làm giảm citrate – là chất bảo vệ chống sỏi. Đề kháng insulin cũng rối loạn cân bằng kiềm toan, thúc đẩy nguy cơ sỏi thận.
Nguy cơ ung thư thận
Béo phì làm tăng insulin máu mạn tính và IGF-1, thúc đẩy tăng sinh tế bào và ức chế cơ chế chết tế bào theo chương trình. Bên cạnh đó, mô mỡ tạo ra môi trường viêm và rối loạn miễn dịch, tạo điều kiện thuận lợi cho sự phát triển của khối u, trong đó có ung thư thận.
Bằng chứng nghiên cứu cho mối liên hệ béo phì và bệnh thận
Nhiều nghiên cứu quy mô lớn trên thế giới đã chứng minh mối liên quan chặt chẽ giữa béo phì và bệnh thận.
Trong nghiên cứu PREVEND năm 2003, Hillege HL và cộng sự theo dõi 7.676 người Hà Lan không mắc đái tháo đường, công bố trên Tạp chí Journal of the American Society of Nephrology, cho thấy BMI cao và phân bố mỡ trung tâm làm tăng nguy cơ albumin niệu vi lượng.
Cùng năm, nghiên cứu Framingham Offspring do Foster MC và cộng sự thực hiện trên 2.676 người trưởng thành, công bố trên cùng tạp chí, ghi nhận BMI cao liên quan sự xuất hiện protein niệu mới.
Ở nhóm người trẻ, nghiên cứu CARDIA năm 2008 do Lewis CE công bố trên Journal of the American Society of Nephrology, với 2.354 người tham gia tuổi 28-40 có chức năng thận bình thường, đã cho thấy béo phì gần như tăng gấp đôi nguy cơ vi đạm niệu, đồng thời chế độ ăn không lành mạnh cũng là yếu tố nguy cơ độc lập.
Nghiên cứu Physicians’ Health năm 2006, do Gelber RP và cộng sự tiến hành trên 11.104 nam giới khỏe mạnh ở Mỹ, đăng trên Journal of the American Society of Nephrology, chứng minh BMI cao tại thời điểm ban đầu và sự gia tăng BMI theo thời gian, đều liên quan nguy cơ xuất hiện eGFR dưới 60mL/phút/1,73m².
Đoàn hệ cựu chiến binh Hoa Kỳ do Hsu CY và cộng sự nghiên cứu năm 2014, với hơn 3,3 triệu đối tượng có eGFR ≥ 60 lúc ban đầu, công bố trên Journal of the American Society of Nephrology, cho thấy BMI trên 30kg/m² liên quan tốc độ suy giảm eGFR nhanh hơn, đặc biệt ở người lớn tuổi.
Nghiên cứu HUNT tại Na Uy năm 2003 với gần 75.000 người trưởng thành, đăng trên Kidney International, báo cáo BMI ≥ 30kg/m² làm tăng nguy cơ tiến triển bệnh thận giai đoạn cuối (end-stage renal disease – ESRD) hoặc tử vong do bệnh thận.
Một nghiên cứu đoàn hệ tại Israel năm 2006 do Vivante A công bố trên New England Journal of Medicine, ở hơn 1,1 triệu thanh thiếu niên nhập ngũ, khẳng định thừa cân lúc tuổi trẻ làm tăng gấp 3 lần nguy cơ ESRD khi trưởng thành, còn béo phì làm tăng nguy cơ gấp 7 lần.
Ngoài ra, nghiên cứu đoàn hệ Kaiser Permanente Northern California năm 2008 với hơn 320.000 người trưởng thành, công bố trên American Journal of Kidney Diseases, cho thấy nguy cơ ESRD tăng tuyến tính theo hạng BMI, kể cả khi hiệu chỉnh đái tháo đường, tăng huyết áp và CKD nền.
Ở lĩnh vực ung thư, nghiên cứu trên 5,24 triệu người trưởng thành tại Anh do Bhaskaran K và cộng sự, công bố năm 2014 trên The Lancet chỉ ra rằng, mỗi 5kg/m² tăng BMI làm tăng 25% nguy cơ ung thư thận, ước tính khoảng 10% số ca ung thư thận quy cho thừa cân và béo phì.
Kết quả này được củng cố bởi một phân tích gộp năm 2014 của Renehan AG và cộng sự trên The Lancet Oncology, bao gồm 221 nghiên cứu (17 nghiên cứu về ung thư thận), cho thấy nguy cơ ung thư thận tăng 24% cho mỗi 5kg/m² tăng BMI và xếp ung thư thận vào nhóm ba loại ung thư chịu tác động lớn nhất từ béo phì.
Tổng hợp lại, các bằng chứng dịch tễ học từ nhiều quần thể và quốc gia cho thấy, BMI cao và béo bụng không chỉ liên quan sự xuất hiện protein niệu, giảm eGFR, tiến triển CKD và ESRD mà còn làm tăng rõ rệt nguy ung thư thận.
Nghịch lý béo phì ở bệnh thận tiến triển
Mặc dù phần lớn bằng chứng đều cho thấy béo phì gây hại cho sức khỏe thận, một hiện tượng nghịch lý đã được quan sát ở bệnh nhân CKD giai đoạn tiến triển và bệnh thận giai đoạn cuối (ESRD), đó là chỉ số BMI cao lại liên quan với tỷ lệ tử vong thấp hơn. Tình trạng tương tự cũng từng được mô tả ở các quần thể bệnh khác như suy tim, COPD, viêm khớp dạng thấp ở người cao tuổi.
Một phần lời giải thích nằm ở hạn chế của BMI, do chỉ số này không phân biệt khối mỡ và khối cơ. Khi các nghiên cứu tách biệt vòng eo hoặc khối cơ với BMI, mối liên hệ bảo vệ với tử vong thường biến mất. Điều này cho thấy, khối cơ cao ở một số bệnh nhân ESRD có thể giải thích một phần hiệu ứng có lợi tưởng chừng đến từ BMI cao.
Tuy vậy, vẫn có dữ liệu gợi ý rằng mỡ dưới da (subcutaneous fat), không phải mỡ nội tạng, có thể mang lại lợi ích nhất định ở nhóm bệnh nhân ESRD với tiên lượng sống ngắn hạn. Ở những bệnh nhân này, cân nặng dư thừa có thể cung cấp dự trữ dinh dưỡng và năng lượng tốt hơn trong bối cảnh bệnh cấp tính.
Nghiên cứu còn cho thấy khối cơ nhiều hơn ở bệnh nhân ESRD có liên quan đến khả năng chống oxy hóa mạnh hơn, nồng độ actin tuần hoàn thấp hơn và mức gelsolin huyết tương cao hơn, đây là các yếu tố liên quan kết cục tốt hơn:
- Actin là một loại protein cấu trúc có mặt rất nhiều trong tế bào, đặc biệt ở cơ tham gia vào việc tạo khung tế bào, co cơ và nhiều quá trình sống khác. Khi tế bào bị tổn thương hoặc chết, actin có thể thoát ra ngoài vào máu. Nồng độ actin tuần hoàn cao thường là dấu hiệu tổn thương mô, có thể gây bất lợi cho cơ thể.
- Gelsolin là một protein điều hòa actin có nhiệm vụ cắt và dọn dẹp actin tự do trong máu, giúp giữ cân bằng hệ thống. Gelsolin còn tham gia vào cơ chế chống viêm, điều hòa quá trình chết tế bào và bảo vệ cơ thể khỏi stress oxy hóa. Nồng độ gelsolin cao hơn thường được xem là có lợi, liên quan đến tiên lượng sức khỏe tốt hơn.
Một số giả thuyết khác giải thích nghịch lý béo phì bao gồm trạng thái huyết động ổn định hơn ở người béo, tăng sản xuất adiponectin và thụ thể hòa tan của TNF-α giúp trung hòa tác hại của TNF-α, cholesterol cao giúp gắn kết endotoxin tuần hoàn và mô mỡ có thể đóng vai trò như bể chứa cô lập độc tố urê.
Điều quan trọng là hiện tượng nghịch lý béo phì dường như chỉ thể hiện lợi ích ngắn hạn, trong khi về lâu dài, mỡ dư thừa vẫn thúc đẩy biến chứng chuyển hóa và tim mạch, làm bệnh thận tiến triển nặng thêm.

Giải pháp phòng ngừa và bảo vệ thận cho người béo phì
Để giảm nguy cơ tổn thương thận, người thừa cân béo phì cần ưu tiên giảm cân theo hướng an toàn và bền vững. Các nghiên cứu cho thấy, việc kết hợp dinh dưỡng khoa học với chế độ ăn giảm calo, giàu rau xanh và protein lành mạnh, cùng với tăng cường vận động thể lực thường xuyên, có thể cải thiện huyết áp, giảm kháng insulin và giảm tình trạng tăng lọc cầu thận, những yếu tố quan trọng trong bảo vệ thận.
Song song đó, cần kiểm soát tốt huyết áp, đường huyết và mỡ máu, vì đây là những yếu tố thúc đẩy mạnh mẽ sự tiến triển của bệnh thận mạn. Bằng chứng từ nhiều phân tích cho thấy, điều trị tăng huyết áp tích cực bằng thuốc ức chế men chuyển (ACEI) hoặc ức chế thụ thể angiotensin (ARB) không chỉ hạ huyết áp mà còn làm giảm protein niệu và bảo vệ thận rõ rệt, đặc biệt ở bệnh nhân béo phì có CKD.
Ngoài ra, việc khám sức khỏe định kỳ và tầm soát chức năng thận đóng vai trò quan trọng để phát hiện sớm tổn thương thận thông qua các xét nghiệm như eGFR và albumin niệu. Hệ thống giám sát CKD tại Anh, sau khi áp dụng rộng rãi hướng dẫn K-DOQI, đã giúp tăng mạnh tỷ lệ phát hiện CKD giai đoạn sớm và cải thiện chất lượng chăm sóc.
Trong một số trường hợp, sử dụng thuốc hỗ trợ giảm cân được FDA Hoa Kỳ phê duyệt có thể được chỉ định, với sự theo dõi chặt chẽ của Bác sĩ chuyên khoa. Các thuốc này vừa hỗ trợ giảm cân, vừa cải thiện kiểm soát đường huyết và giảm áp lực chuyển hóa lên thận.
Ở những bệnh nhân béo phì mức độ nặng, đặc biệt khi có CKD và chuẩn bị ghép thận, phẫu thuật dạ dày giảm cân – bariatric cũng có thể được cân nhắc như một giải pháp hỗ trợ.


* Voucher chỉ áp dụng cho khách hàng thăm khám lần đầu tiên tại Phòng khám MedFit
Các thuốc giảm cân được FDA Hoa Kỳ phê duyệt và tác động trên bệnh thận
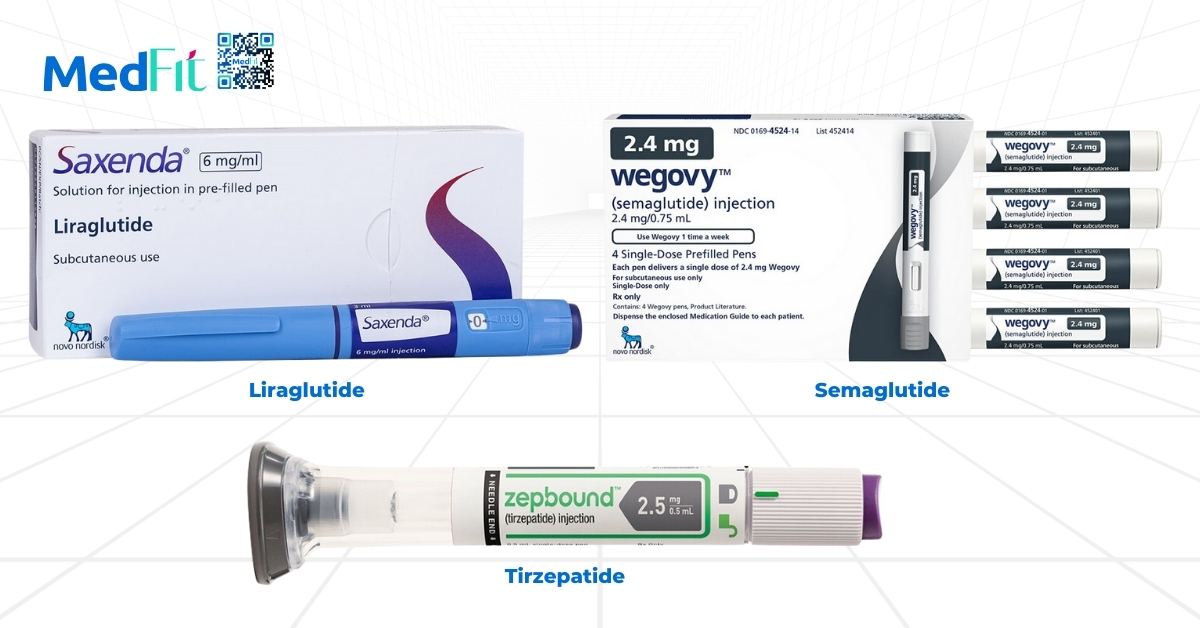
Hiện có các thuốc quản lý cân nặng dài hạn được FDA Hoa Kỳ phê duyệt gồm orlistat, phentermine – topiramate, naltrexone – bupropion, nhóm đồng vận thụ thể GLP-1 như liraglutide, semaglutide và tirzepatide.
Danh mục này được nêu nhất quán trong tổng quan gần đây của Viện Quốc gia về Đái tháo đường, Tiêu hóa và Bệnh thận Hoa Kỳ (National Institute of Diabetes and Digestive and Kidney Diseases – NIDDK), giúp định vị đúng vai trò từng nhóm trong điều trị béo phì mạn tính.
Nhóm đồng vận thụ thể GLP-1 (GLP-1 receptor agonist)
Nhóm đồng vận thụ thể GLP-1 giúp giảm cân đáng kể nhờ giảm cảm giác thèm ăn và làm chậm làm rỗng dạ dày, đồng thời cải thiện kiểm soát đường huyết. Ở mức thận, GLP-1 cho thấy các hiệu ứng có lợi như giảm albumin niệu, chống viêm mức độ tế bào, giảm stress oxy hóa và cải thiện chức năng ống kẽ.
Bằng chứng lâm sàng từ các thử nghiệm tim mạch lớn đã ghi nhận lợi ích thận, như tác động lên biến cố thận gộp:
- Trong nghiên cứu LEADER với liraglutide và SUSTAIN-6 với semaglutide, nguy cơ biến cố thận do đái tháo đường giảm chủ yếu nhờ giảm mới xuất hiện albumin niệu dai dẳng, bên cạnh tín hiệu chậm suy giảm eGFR.
- Thử nghiệm FLOW công bố trên New England Journal of Medicine cho thấy, semaglutide ở bệnh nhân đái tháo đường típ 2 kèm bệnh thận mạn làm giảm rõ rệt kết cục thận gộp, gồm suy thận giai đoạn cuối, giảm bền vững eGFR hoặc tử vong do nguyên nhân thận, đồng thời giảm tử vong tim mạch. Kết quả này là nền tảng cho động thái mở rộng chỉ định bảo vệ thận ở bệnh nhân đái tháo đường có CKD.
- Với người béo phì có rối loạn chuyển hóa sớm, hiệu quả giảm cân của semaglutide trong chương trình STEP đi kèm cải thiện huyết áp và đường huyết, từ đó giảm các yếu tố thúc đẩy tăng lọc cầu thận và tổn thương thận.
Ở hướng thuốc mới hơn, tirzepatide là chất chủ vận kép GIP và GLP-1, đã chứng minh giảm cân vượt trội và có tín hiệu lợi ích thận.
Một phân tích bổ sung được tiến hành sau khi thử nghiệm SURPASS-4 kết thúc, nhằm rút ra thêm thông tin hoặc làm sáng tỏ tác động của thuốc tirzepatide trên bệnh thận, cho thấy tirzepatide giảm albumin niệu và làm chậm suy giảm eGFR so với insulin nền, gợi ý khả năng làm chậm tiến triển CKD.
Tuy vậy, vẫn cần thêm các nghiên cứu lâm sàng chuyên biệt về thận để khẳng định chắc chắn.
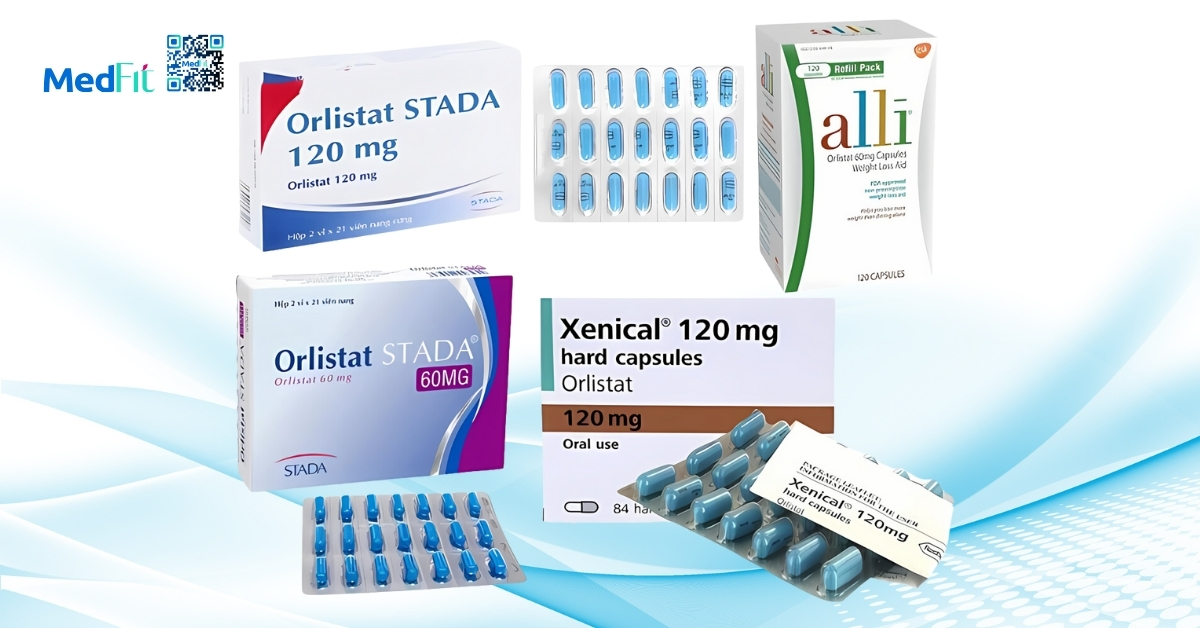
Orlistat
Orlistat hầu như không hấp thu vào tuần hoàn nên an toàn về mặt toàn thân, nhưng có báo cáo trường hợp và chuỗi ca về tăng hấp thu oxalat đường ruột, dẫn tới tăng canxi oxalat niệu, sỏi thận và thậm chí viêm thận kẽ do oxalat.
Khi dùng ở người có tiền sử sỏi, nên tư vấn uống đủ nước, đảm bảo canxi khẩu phần để gắn oxalat trong ruột và tái đánh giá nếu có triệu chứng đường tiểu.
Phentermine – topiramate
Phentermine – topiramate có hiệu quả giảm cân tốt nhưng phần topiramate có thể làm toan chuyển hóa mức nhẹ, hạ citrate niệu và tăng nguy cơ sỏi. Một số dữ liệu dịch tễ gần đây còn gợi ý mối liên hệ bất lợi về thận khi dùng riêng rẽ phentermine hoặc topiramate trong bối cảnh béo phì, vì vậy cần sàng lọc nguy cơ sỏi và theo dõi triệu chứng tiết niệu khi kê đơn.

Naltrexone – bupropion
Naltrexone – bupropion giúp kiểm soát ăn uống theo hướng hành vi nhưng có thể làm tăng nhẹ huyết áp và nhịp tim, điều này quan trọng ở người béo phì có nguy cơ thận vì kiểm soát huyết áp là trụ cột bảo vệ thận.
Dù chưa có thử nghiệm thận chuyên biệt, thuốc này được nêu trong khuyến nghị quản lý cân nặng dài hạn của NIDDK và thường được cân nhắc khi mục tiêu chính là kiểm soát ăn uống bốc đồng.
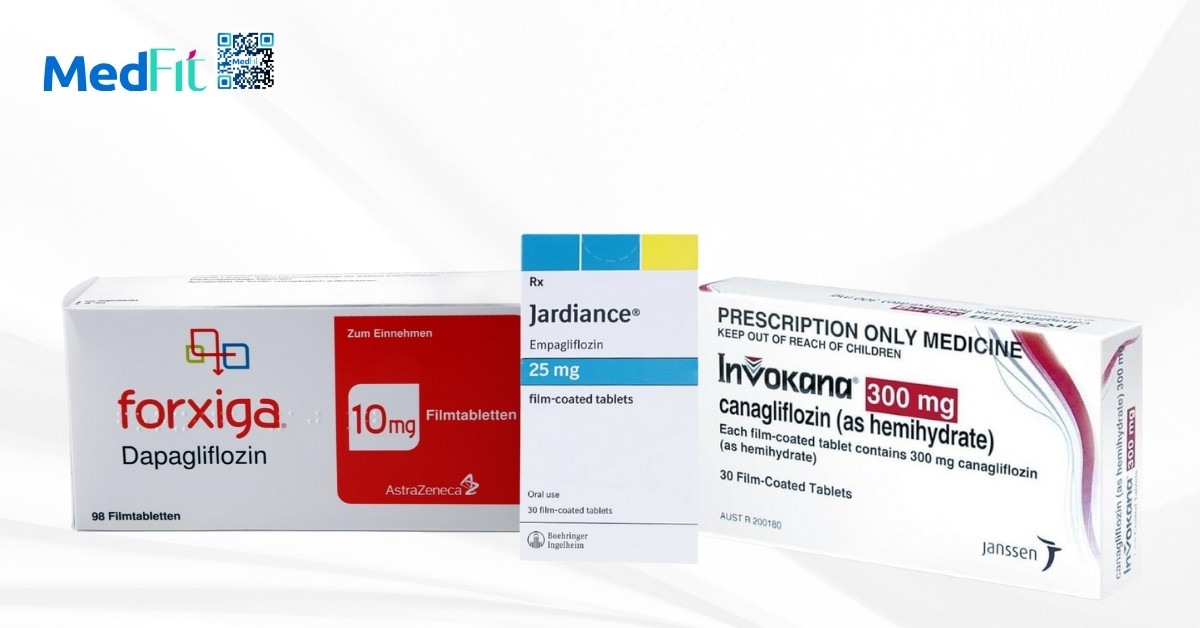
Thuốc ức chế kênh SGLT2
Thuốc ức chế kênh SGLT2 làm tăng thải natri và glucose qua nước tiểu, giúp phục hồi tín hiệu ống cầu thận, co tiểu động mạch vào, từ đó giảm áp lực nội cầu thận và giảm hiện tượng tăng lọc có hại. Tác dụng cơ chế này xuất hiện sớm và không phụ thuộc hoàn toàn vào mức đường huyết, vì vậy SGLT2 thể hiện lợi ích thận nhất quán ở cả bệnh nhân có hoặc không có đái tháo đường.
Nghiên cứu DAPA-CKD chứng minh dapagliflozin giảm mạnh nguy cơ suy giảm bền vững eGFR, tiến tới bệnh thận giai đoạn cuối và tử vong do thận hoặc tim mạch trên nền điều trị chuẩn, bao gồm bệnh nhân không đái tháo đường.
Nghiên cứu EMPA-KIDNEY mở rộng lợi ích này cho empagliflozin ở quần thể CKD đa dạng, hạ nguy cơ kết cục thận chính và làm chậm dốc eGFR. Trước đó, CREDENCE đã xác lập lợi ích bảo vệ thận của canagliflozin ở bệnh nhân đái tháo đường típ 2 và albumin niệu cao.
Trên lâm sàng, SGLT2 nên được cân nhắc sớm ở người thừa cân béo phì có CKD hoặc có albumin niệu dù đường huyết chưa quá cao, phối hợp nền tảng với ức chế hệ renin angiotensin. Cần theo dõi thể tích tuần hoàn, nguy cơ nhiễm nấm sinh dục và hiếm gặp hơn là toan ceton euglycemic ở người ăn rất ít carbohydrate hoặc giảm insulin nhanh.
Cuối cùng, cần lưu ý rằng thuốc ức chế SGLT2 không phải là thuốc giảm cân được FDA Hoa Kỳ phê duyệt. Do đó, SGLT2 thường được phối hợp với GLP-1 hoặc các thuốc hỗ trợ giảm cân khác. Sự kết hợp này giúp vừa bảo vệ thận trên bệnh nhân béo phì có bệnh thận thông qua việc giảm gánh nặng ở cầu thận, vừa cải thiện chuyển hóa liên quan đến cân nặng.
Béo phì không chỉ là vấn đề thẩm mỹ mà thực sự là một bệnh lý mạn tính, tác động đến gần như mọi cơ quan trong cơ thể, trong đó có thận. Nhiều bằng chứng khoa học đã chỉ ra rằng, béo phì làm tăng nguy cơ tổn thương cầu thận, thúc đẩy bệnh thận mạn và cả suy thận giai đoạn cuối.
Việc duy trì cân nặng hợp lý, kiểm soát huyết áp, đường huyết và mỡ máu là những bước quan trọng để bảo vệ chức năng thận. Hành trình giảm cân bền vững cần sự đồng hành của chuyên gia.
Tại MedFit, đội ngũ Bác sĩ đa chuyên khoa và chuyên gia dinh dưỡng sẽ xây dựng phác đồ cá nhân hóa, kết hợp dinh dưỡng, vận động và liệu pháp y khoa tiên tiến, giúp kiểm soát cân nặng an toàn, giảm gánh nặng lên thận và cải thiện sức khỏe toàn diện.
Nếu đang lo ngại về cân nặng hoặc muốn tìm giải pháp giảm mỡ khoa học, hãy để MedFit đồng hành cùng bạn trên hành trình thay đổi. Đặt lịch tư vấn cùng MedFit ngay hôm nay để bắt đầu hành trình thay đổi an toàn và bền vững. 

Tài liệu tham khảo
- Tchang BG, Aras M, Kumar RB, et al. Pharmacologic Treatment of Overweight and Obesity in Adults. [Updated 2024 Aug 20]. In: Feingold KR, Ahmed SF, Anawalt B, et al., editors. Endotext [Internet]. South Dartmouth (MA): MDText.com, Inc.; 2000-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK279038/
- Chang AR, Chen Y, Still C, et al. Bariatric surgery is associated with improvement in kidney outcomes. Kidney Int. 2016;90(1):164-171. doi:10.1016/j.kint.2016.02.039
- Chronic Kidney Disease Surveillance Team. Implementation of K-DOQI guidelines in UK primary care and its impact. Kidney International. 2006;69(12):2094–2100
- Gerstein HC, Colhoun HM, Dagenais GR, et al. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet. 2019;394(10193):121-130. doi:10.1016/S0140-6736(19)31149-3
- Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2020;383(15):1436-1446. doi:10.1056/NEJMoa2024816
- Rafat C, Doreille A. Could Plasmodium falciparum-related kidney disease stand as another example of interferonopathy?. Kidney Int. 2022;102(3):669-670. doi:10.1016/j.kint.2022.06.009
- Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 2024;105(4S):S117-S314. doi:10.1016/j.kint.2023.10.018
- Kovesdy CP, Furth SL, Zoccali C; World Kidney Day Steering Committee. Obesity and Kidney Disease: Hidden Consequences of the Epidemic. Can J Kidney Health Dis. 2017;4:2054358117698669. Published 2017 Mar 8. doi:10.1177/2054358117698669
- Look AHEAD Research Group, Wing RR, Bolin P, et al. Cardiovascular effects of intensive lifestyle intervention in type 2 diabetes. N Engl J Med. 2013;369(2):145-154. doi:10.1056/NEJMoa1212914
- Marso SP, Bain SC, Consoli A, et al. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med. 2016;375(19):1834-1844. doi:10.1056/NEJMoa1607141
- Marso SP, Daniels GH, Brown-Frandsen K, et al. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2016;375(4):311-322. doi:10.1056/NEJMoa1603827
- Andrew Levey. What’s New About the New CKD Guideline?. [online] Available at: What’s New About the New CKD Guideline? | National Kidney Foundation [Accessed 10 October 2025]
- NIH: National Institute of Diabetes and Digestive and Kidney Diseases. Prescription Medications to Treat Overweight & Obesity. [online] Available at: Prescription Medications to Treat Overweight & Obesity – NIDDK [Accessed 10 October 2025]
- Phuc TT, Duc TQ, Quynh Chi VT, Quang PN. The prevalence of excess weight among Vietnamese adults: A pooled analysis of 58 studies with more 430 thousand participants over the last three decades. Nutr Health. 2023;29(3):443-452. doi:10.1177/02601060221129440
- Mallamaci F, Ruggenenti P, Perna A, et al. ACE inhibition is renoprotective among obese patients with proteinuria. J Am Soc Nephrol. 2011;22(6):1122-1128. doi:10.1681/ASN.2010090969
- The EMPA-KIDNEY Collaborative Group, Herrington WG, Staplin N, et al. Empagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2023;388(2):117-127. doi:10.1056/NEJMoa2204233
- World Health Organization (WHO). Obesity and overweight. [online] Available at: Obesity and overweight [Accessed 10 October 2025]
- WHO Expert Consultation. Appropriate body-mass index for Asian populations and its implications for policy and intervention strategies. Lancet. 2004;363(9403):157-163. doi:10.1016/S0140-6736(03)15268-3
- Wilding JPH, Batterham RL, Calanna S, et al. Once-Weekly Semaglutide in Adults with Overweight or Obesity. N Engl J Med. 2021;384(11):989-1002. doi:10.1056/NEJMoa2032183
- Navaneethan SD. Trials and Tribulations in Studying Kidney Outcomes With Intentional Weight Loss. Circulation. 2019;139(3):376-379. doi:10.1161/CIRCULATIONAHA.118.038677













